2021年12月9日,来自美国哈佛和麻省理工博德研究所的Alex K. Shalek团队在Cell上在线发表题为Microenvironment drives cell state, plasticity, and drug response in pancreatic cancer 的文章,开发并采用优化的转化工作流程,使用单细胞RNA测序(scRNA-seq)对转移性PDAC患者组织及匹配的类器官模型进行了高分辨率分析,生成了转移性PDAC的单细胞图谱,并将其作为匹配的类器官模型中细胞中状态的标准化参考,由此发现了一种新的中间共表达子(IC)PDAC细胞状态,揭示了不同的位点和亚型特异性TME,并证明TME信号是癌细胞状态、可塑性和对治疗反应的关键调节因子。

目前的精准医学方法专注于评估模型的DNA保真度,而忽略了RNA状态。因此,本文研究人员比较了原发和转移性患者肿瘤与已建立的细胞系和新产生的患者源性类器官队列的DNA和RNA测序谱,以了解每个模型系统如何代表突变和RNA表型在患者中的分布。分析结果显示,各组之间的驱动癌基因改变频率没有显著差异,但是PDAC细胞系和类器官均不能完全显示患者队列中出现的全部表达亚型,提示体外模型系统保留了遗传保真度,但失去了表达状态异质性。这就迫切需要新的方法以用来识别体内和体外模型体系中癌细胞状态的决定因素。为此,研究人员建立了一种方法,利用PDAC患者的核心穿刺活检构建匹配的类器官,并对两者进行匹配的scRNA-seq(图1),从而获得了高质量的恶性和非恶性单细胞转录组。
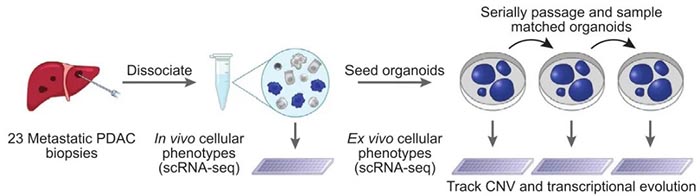
图1
通过拷贝数变异(CNV)分析将PDAC细胞与非恶性细胞分离后,研究人员首先分析了之前描述的RNA亚型是否在转移性PDAC单细胞中表达。结果显示,转移细胞亚群在来自独立批量研究的经典样或基础样特征方面表达较高,表明这些表达程序与体内PDAC生物学的普遍相关性。而其余的文献来源的特征在这些转移细胞中表达较低,提示要么是原发性疾病的特异性,要么是大量RNA谱中非恶性表达的影响。有趣的是,有一大群细胞对所有先前提出的特征都表现出低表达,这突出了我们对PDAC表达状态的理解上的差距。进一步分析表明,并非所有具有基础样特征的细胞都具有相同的潜在属性,由此强调了利用scRNA-seq来了解恶性细胞如何感知和响应其局部TME的重要性。
本文将来自单细胞队列的特征称为单细胞基础特征(scBasal)和单细胞经典特征(scClassical)。虽然一些研究表明基础的和经典的程序仅存在于离散的细胞群中,但本研究发现scBasal和scClassical的程序并不是相互排斥的。相反,研究人员发现了介于scBasal和scClassical基因表达特征之间的细胞,它们在不同程度上共同表达了这两个程序的特征。同时研究人员鉴定了115个表达与scBasal-scClassical共表达相关的基因,并将其命名为IC状态。分析表明,虽然IC状态可能并不代表发育轨迹上的一个明显步骤,但它可能代表了癌症环境中类似的应激诱导的过渡状态。恶性细胞状态多样性较高的样本(即scBasal细胞和scClassical细胞比例较高)也表现出表达IC状态的细胞比例较高,这表明IC状态可能是scBasal细胞和scClassical细胞之间的过渡。进一步研究结果表明,转移性和原发性PDAC中存在一个三重细胞状态框架,在单细胞中跨越了基础表型和经典表型,并具有相当大的共同表达的特征。
随后,研究人员分析了匹配的体外模型是否保留了其来源组织的细胞状态分布,研究结果表明微环境生长条件的改变显著改变了细胞转录状态,并诱导了培养特异性表达程序,由此也强调了利用匹配的体内状态作为参考对体外模型进行标准化的重要性。无论原始活检中的细胞状态分布如何,在培养过程中,单个模型都随着时间的推移出现了更多的scClassical或类器官特异性细胞状态。进一步探索这种细胞状态偏差的驱动因素发现,虽然与之前的大量研究结果一致,单细胞KRAS拷贝数增加与转移细胞中的scBasal显著相关,但是恶性细胞状态从体内的scBasal转换成了类器官培养中的scClassical状态,由此表明单靠KRAS扩增不足以锁定scBasal表达状态,PDAC细胞是可塑的,在这种情况下,微环境可以独立于基因型而影响细胞状态。
深入的实验发现,培养基配方会影响体外PDAC的转录状态。在类器官培养中会出现某些基因的相对缺失,这些基因在体内转录亚型的表达差异表明,TME信号在充分明确的癌细胞转录状态和潜在的治疗反应中发挥了作用,即使是已建立的模型也对培养条件的变化敏感,并且预先选择压力和培养基印记的组合形成了现存模型系统中的细胞状态偏差,影响了它们的功能属性。通过调节培养条件可以实现跨越纯scClassical表达、异质性表达和纯scBasal表达的成分差异,类似于在体内看到的那些。此外,实验还发现,转录状态可能是肿瘤对药物反应的主要决定因素,而细胞状态的差异靶向性代表了一种可操作的治疗模式。添加TME信号或改变培养基配方,可以通过改变转录状态影响肿瘤模型对药物的敏感性,这也凸显了肿瘤模型本身的显著表型和功能可塑性。
肿瘤细胞体内TME相关表达模式的存在提示转移性TME可能存在亚型依赖结构和信号转导。研究人员在转移性TME中观察到不同的免疫和基质细胞类型,并且确定了与原发性疾病相比的肝脏生态位所特有的间充质特征。进一步分析则表明癌细胞状态和局部TME之间存在着协调关系,在基础环境中免疫细胞多样性减少。体内实验与类器官研究均表明TME提供的细胞因子和免疫激活在指导癌细胞状态中发挥着关键作用。
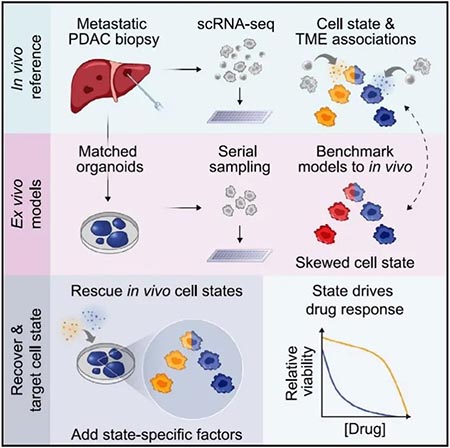
图2
综上所述,本研究提供了一个可用于在患者来源的肿瘤模型系统中对细胞状态进行标准化评估、识别转录可塑性驱动因素以及评估其在模型系统中的功能意义的系统框架(图2),该方法将为系统评估细胞状态以作为癌症靶向特征提供新途径。
原文链接:
https://doi.org/10.1016/j.cell.2021.11.017













