
导读
组织驻留的干细胞衰老导致干细胞衰竭,是引起生理和病理老化的主要原因。干细胞来源的细胞外囊泡(SC-EVs)在临床前研究中被报道对多种疾病具有治疗潜力。然而,尚不清楚SC-EVs是否能使衰老的组织干细胞恢复活力,以预防年龄相关的疾病。在这里,作者研究发现人类胚胎干细胞衍生的小细胞外囊泡(hESC-sEVs)的长期应用可挽救衰老的骨髓间充质干细胞(BM-MSC)的功能,并防止衰老小鼠中与年龄相关的骨质流失。转录组分析显示,hESC-sEVs治疗上调了BM-MSCs抗衰老、干细胞增殖和成骨分化相关基因的表达。此外,液相色谱串联质谱(LC-MS/MS)分析鉴定了4122个包裹在hESC-sEVs中的蛋白。生物信息学分析预测,hESCs-sEVs中的蛋白成分协同作用,诱导激活几个典型信号通路,包括Wnt、Sirtuin、AMPK、PTEN信号通路,导致BM-MSCs抗衰老基因的上调,进而恢复衰老的BM-MSCs功能。总的来说,作者的发现揭示了hESC-sEVs在逆转BM-MSCs衰老和年龄相关的成骨功能障碍方面的作用,从而防止了年龄相关的骨丢失。由于hESC-sEVs可以缓解组织驻留干细胞的衰老,它们可能是有希望的治疗年龄相关疾病的候选药物。
论文ID
题目:Human ESC-sEVs alleviate age-related bone loss by rejuvenating senescent bone marrow-derived mesenchymal stem cells
译名:人ESC-sEVs通过恢复衰老的骨髓间充质干细胞来缓解与年龄相关的骨丢失
期刊:JOURNAL OF EXTRACELLULAR VESICLES
IF:14.976
发表时间:2020.10.10
通讯作者单位: 上海交通大学附属第六人民医院
DOI号:https://doi.org/10.1080/20013078.2020.1800971
主要内容
首先,作者对本研究中使用的人类胚胎干细胞(hESCs)进行了表征。hESC阳性表达多能性相关标志物,包括OCT4,NANOG,SSEA4,TRA-1-60和TRA-1-81。然后从hesc衍生的条件培养基中分离出sEVs,并根据形态、颗粒大小和浓度以及表面标记进行表征。TEM显示纯化后的hESC-sEVs大小约为100 nm,呈杯状形态。Western blotting分析显示,hESC-sEVs中CD9、CD63和TSG101呈阳性,而golgi相关蛋白GM130呈阴性。此外,hESC-sEVs的收率根据颗粒浓度和蛋白浓度进行评估。
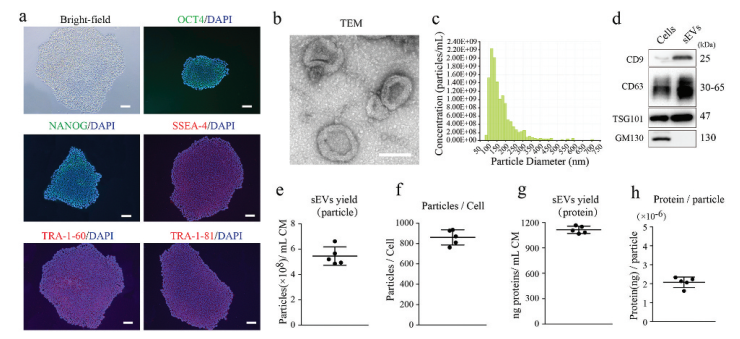
图一:hESCs和hESC-sEVs的特征
然后作者探讨了hESC-sEVs在预防年龄相关骨丢失中的作用。为了追踪体内hESC-sEVs的生物分布,作者给SAMP8小鼠注射了dirl标记的hESC-sEVs(1 1010颗粒/mL, 100 mol / l),在给药后6、12、24和48小时对其进行安乐死和解剖器官的体外成像。荧光信号可以首先观察股骨和胫骨后6小时的管理。随着观察时间的延长,骨内荧光信号逐渐增加,并在给药后48小时达到峰值。同时在胃肠道、肝、脾、肾、心、肺等部位均可见高信号。接下来,6个月大的雄性SAMP8小鼠被给予6个月的hESC-sEVs。小鼠被随机分为对照组和hESC-sEVs治疗组。治疗6个月后,处死小鼠,取股骨进行显微ct和组织学分析。与经药物处理的小鼠相比,经sevs处理的小鼠表现出更健康的外观和状态。这些结果表明,hESC-sEVs治疗可以防止体内年龄相关的骨丢失。
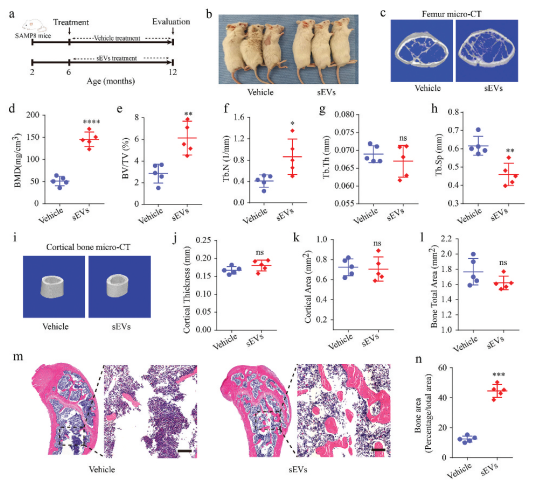
图二:在SAMP8小鼠中,hESC-sEVs治疗可防止年龄相关的骨丢失
总结
综上所述,作者证明了hESC-sEVs在逆转BM-MSCs衰老、通过封装蛋白转移促进其增殖和成骨分化潜能方面具有积极作用。hESC-sEVs中的蛋白质成分通过直接或间接的相互作用,或通过激活几个参与减缓细胞衰老和促进成骨的典型信号通路来调节抗衰老基因的表达。这些发现不仅强调了从干细胞中提取的ev在预防与年龄相关的骨丢失方面的有效性,而且也为衰老的干细胞的再生和有希望治疗与年龄相关的疾病开辟了一条途径。
原文链接
https://doi.org/10.1080/20013078.2020.1800971
参考文献
1.López-Otín C, Blasco MA, Partridge L, et al. The hallmarks of aging. Cell. 2013;153(6):1194–1217.













