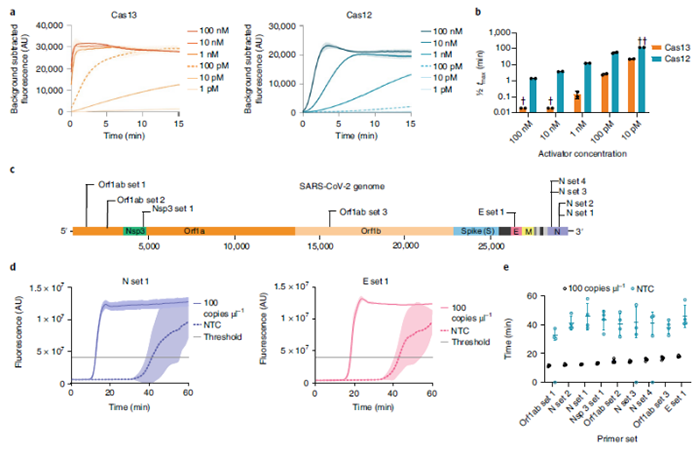
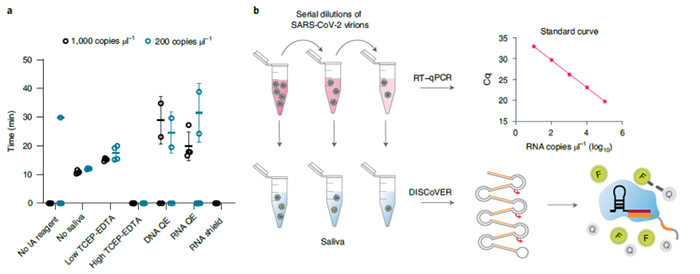
2022年8月11日,诺奖得主、加州大学伯克利分校 Jennifer Doudna,以及 David Savage 和 Patrick Hsu 团队,在 Nature 子刊 Nature Biomedical Engineering 上发表了题为:Rapid detection of SARS-CoV-2 RNA in saliva via Cas13 的研究论文。该研究报告了一种高敏感性和高特异性的快速检测新冠病毒的方法——DISCoVER,无需提取 RNA,就可以检测出唾液中的 SARS-CoV-2。首先,研究者试图比较 Cas13 和 Cas12 酶的核酸检测特性,评估了 Leptotrichia buccalis Cas13a(LbuCas13a)和 Lachnospiraceae bacterium ND2006 Cas12a(LbCas12a)的报告酶切割活性,并在其相应的合成活化剂分子稀释系列中,使用匹配的引导 RNA 间隔序列。结果显示 LbuCas13a 在低活化剂浓度下的检测速度明显快于 LbCas12a。为了达到更高的灵敏度,研究者选择了环介导等温扩增技术(LAMP)作为一种经济高效的核酸扩增方法。LAMP 使用逆转录酶、链置换 DNA 聚合酶和三组引物,将病毒 RNA 转化为 DNA 底物。由于 Cas13 靶向单链 RNA,而 LAMP 扩增 DNA 底物,研究者采用了 LAMP 产物的转录来实现底物的兼容性。将 T7 RNA 聚合酶启动子序列整合到 LAMP 引物序列,用于后续的转录和 Cas13 检测,研究者将此称为 rLAMP。经测试,T7 启动子在 rLAMP 扩增子中正确掺入并发挥作用。为了确认 DISCoVER 检测方法的可复制性,研究者在 8 个 mBIP rLAMP 反应重复中测试了 Cas13 检测,其中 RNA 在 20 μl 反应体系中的浓度为 100 拷贝/μl。所进行的八次重复中阳性样本信号均是阴性对照的 25 倍以上,保持很好的稳定性。接下来,研究者试图确定 DISCoVER 对唾液样本的分析灵敏度和特异性。对一系列病毒浓度进行了 20 次 DISCoVER 重复检测后,确定了唾液中病毒检测的最低浓度为 40 拷贝/μl。为了测定 DISCoVER 的特异性,对来自 30 个 SARS-CoV-2 阴性的不同个体的唾液样本进行了测试,没有出现任何假阳性信号。接下来,研究者中使用 DISCoVER 验证了从患者呼吸道拭子样本中提取的总 RNA。结果显示,DISCoVER 对提取的 RNA 的敏感性为 93.9%,特异性为 100%。此外,研究者观察到 PPV 为 100%,NPV 为 93.75%。最后,研究者开发了一种紧凑型便携式微流体设备,可在即时护理应用的环境中进行检测。该化学反应适用于在重力驱动的微流控盒上运行,具有温度控制的反应和检测室。该装置包含用于控制流体流动的排气泵、用于 rLAMP 室的电阻加热器和用于 Cas13 室冷却和加热的热电冷却器/加热器(TEC)。测定荧光检测由紧凑型定制检测器进行,用于实时样品读数。
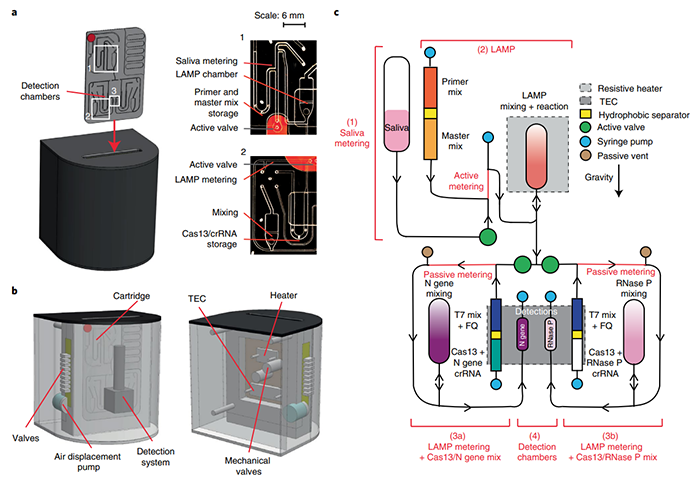
研究者对 DISCoVER 设备进行了实验验证。重新测试了三个阴性和三个阳性呼吸道临床样本。在所有三个阳性样本中均正确检测到了 SARS-CoV-2,并且在所有三个阴性样本中仅检测到 RNase P 信号。然后,研究者对 10 个经 RT-qPCR 检测为 COVID-19 阳性的现场收集的临床唾液样本和 3 个阴性唾液样本进行了检测,进一步验证了该设备的稳健性和可重复性。本研究开发了一种新的 SARS-CoV-2 检测方法——DISCoVER 检测,建立了不需要提取 RNA 的检测流程,可以对唾液中的 SARS-CoV-2 进行检测。DISCoVER 检测结合了 30 分钟的 rLAMP 步骤,然后是 T7 转录和基于 Cas13 的检测,灵敏度和特异性极高,实现了快速检测。敏感的核酸扩增与 CRISPR 介导的特异性和可编程性相结合,有可能为多种病原体检测提供灵活的诊断。与咽拭子或鼻拭子样本相比,唾液样本的采集更具舒适性。同时,唾液采集可能不需要医务人员进行,因此更能节约样品采集所需的人力,也使得该研究成果更具有应用推广的价值。https://www.nature.com/articles/s41551-022-00917-y