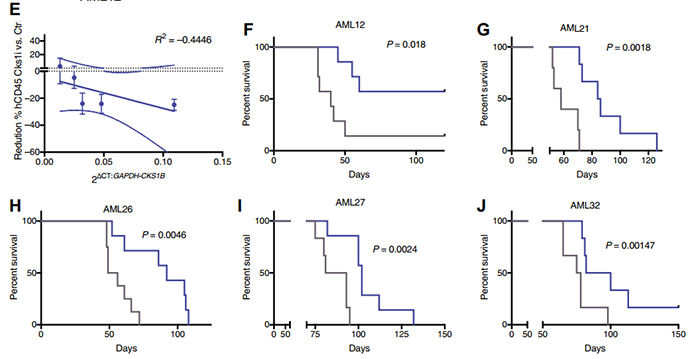
2022年6月22日,来自英国弗朗西斯·克里克研究所的Dominique Bonnet团队在Science Translational Medicine杂志上发表了一篇题为 CKS1 inhibition depletes leukemic stem cells and protects healthy hematopoietic stem cells in acute myeloid leukemia 的文章,他们证明了通过单一抑制CKS1依赖性蛋白质降解或结合标准化疗在减少LSC池方面的功效,相比之下,CKS1抑制对正常造血具有相反的作用,改善干细胞功能并赋予对化学治疗毒性的保护作用。总之,这些发现提供了一种新的治疗方法,可以根除耐药性LSCs并保持健康的造血功能。CKS1B的过表达与多种实体瘤的不良预后相关,其表达在正常和恶性造血之间以及不同造血亚型之间存在显著差异。研究人员假设AML中的CKS1B高表达可能对通过SCFSKP2-CKS1 E3连接酶抑制剂(以下简称为CKS1i)抑制CDK-CKS1依赖性磷酸化或SCF-CKS1依赖性蛋白质降解提供选择性易感性。为此,他们筛选出一批涵盖多种形态学和分子亚型的AML患者样本,测试对一系列CDK抑制剂、广谱蛋白降解抑制剂和CKS1i的敏感性,后两者能显著增强前者引起的药物易感性(DSS)。如果将AML患者样本移植到NSG小鼠中以测试体内影响,发现CKS1i能显着降低移植携带最高CKS1B表达的AML患者样本的小鼠白血病负担,总生存期有所提高。
图1. 接受或不接受CKS1i的AML异种移植小鼠生存曲线(深蓝色代表接受治疗,黑色代表未接受)
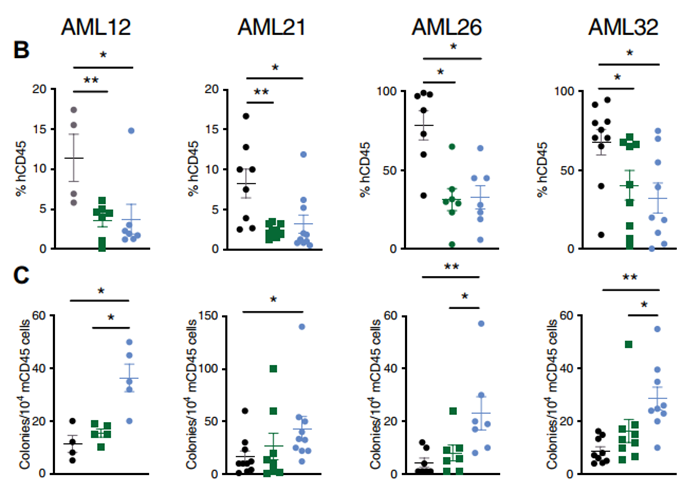
在CKS1Blow AML异种移植小鼠中观察到CKS1i治疗对骨髓定植和总体存活的影响可能表明CKS1i对LSCs的特定作用机制。为了更好地量化LSCs在原发性AML患者中对CKS1的依赖性,他们在单细胞分辨率下测定出CKS1蛋白丰度与一系列免疫表型和功能性LSCs标记密切相关。此外,无论在体内还是体外培养条件下,CKS1i处理都会引起LSCs频率降低。有趣的是,研究人员将健康脐带血衍生的CD34+细胞移植到NSG小鼠中,在存或不存在CKS1i的情况下用临床化疗方案处理小鼠发现CKS1i能够避免化疗引起的正常造血细胞死亡以及HSCs频率增加,并且能够挽救化疗引起的严重的肠道毒性副作用,说明CKS1i诱导的生长抑制对健康组织具有化学保护作用。那么引起健康和恶性细胞对CKS1i不同反应的机制是什么呢?通过蛋白组学分析,研究人员发现CKS1B表达和CKS1i反应之间的直接相关性,关键的差异蛋白被富集到Wnt信号传导、细胞周期调控和NFκB信号通路中。此外,代谢活性标志物如mTORpS2448、炎症反应如包括 NFκBpS529的减少等导致CKS1i处理的CD34+细胞中蛋白质翻译减少,这些信号通路是控制应激反应的基础,对于防止HSCs中致命的ROS积累尤为重要。另外,研究人员发现在CKS1i处理后,AML细胞中总RAC1蛋白丰度增加,以及NADPH的剂量依赖性增加,进而引起细胞中的ROS积累增加。如果使用抗氧化剂NAC处理AML细胞,则能减少ROS累积并逆转CKS1i依赖性的活力降低,说明CKS1i通过驱动致死ROS积累进而杀死AML细胞。接下来,研究人员将具有CKS1B不同表达水平的原发性AML患者样本移植到NSG小鼠中,分别用化疗或CKS1i联合化疗的方式处理小鼠。化疗后一周,无论CKS1B表达如何,异种移植物在两组中的人CD45+细胞负担均显着降低,但从联合治疗组小鼠中提取的常驻鼠CD45+细胞具有更高的集落形成潜力。此外,化疗仅能够提高一只移植小鼠存活率,但联合疗法能提高所有小鼠总体存活期长达至150天。图2. 两种疗法均能降低AML负担(B)但只有联合疗法能维护正常HSPCs的集落形成能力(C)。总之,这项工作击破了选择性靶向CSCs的同时保留正常干细胞的癌症治疗的主要挑战,抑制CKS1依赖性蛋白降解对于AML而言具有极大的治疗潜力,既可作为CKS1B高表达的AML的单一药物,也可与化疗联合使用。除了AML之外,CKS1B过表达与其他实体癌类型的相关性报告提示这种方法可能存在广适性。http://doi.org/10.1126/scitranslmed.abn3248