导读
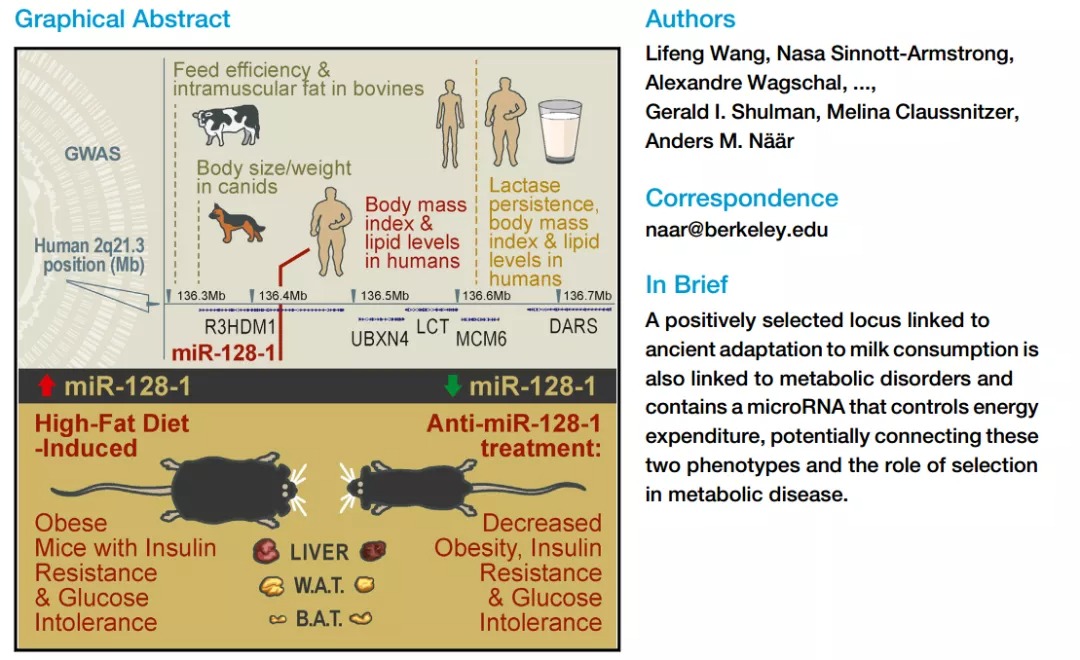
欧洲人在含有乳糖酶基因的2q21.3位点的阳性选择,被认为是远古时期成年人消化牛奶的能力在饥荒中幸存的选择。然而,2q21.3基因座也与人类的肥胖和2型糖尿病有关,这增加了该基因座额外的基因元素可能通过促进能量储存,促进了对饥荒的进化适应,但现在赋予了代谢疾病的易感性。作者在这里表明,位于正向选择位点中心的miR-128-1 microRNA在哺乳动物中代表了一个重要的代谢调节因子。在小鼠代谢性疾病模型中,对miR-128-1的反义靶向和基因消融可增加能量消耗,改善高脂饮食诱导的肥胖,并显著提高糖耐量。与依赖mir -128-1的能量储存相关的节俭表型可能与古代对饥荒的适应和现代与营养过剩相关的代谢失调有关。
论文ID
题目:A MicroRNA Linking Human Positive Selection and Metabolic Disorders
译名:MicroRNA连接人类积极选择和代谢障碍。
期刊:Cell
IF:38.637
发表时间:2020.10.13
通讯作者单位: 麻省总医院癌症中心
DOI号:https://doi.org/10.1016/j.cell.2020.09.017
主要内容
作者首先发现欧洲长单倍型在2q21.3与基因座范围内的染色质可及性增加有关,这导致miR-128-1和基因共表达基因在该基因座的协同升高的表达。鉴于miR-128-1通过分化和贮库物特异性表达增加的表达,作者将脂肪以及可能的其他代谢组织牵连到这种效应中。为了探讨miR-128-1是否在调节能量消耗和代谢控制中发挥作用,作者首先在高脂饮食(HFD)喂养的雄性C57BL/6J小鼠中检测了anti-miR寡核苷酸对miR-128-1的抑制作用,这是一个建立的饮食诱导肥胖(DIO)模型。雄性DIO小鼠每周皮下注射10 mg / kg锁定miA-128-1的锁定核酸(LNA)修饰的抗miR,在16周内有效降低了代谢组织中miR-128-1的水平, 伴随着HFD体重的大幅减少,在治疗开始后2周就很明显了。总之,Anti-miR寡核苷酸可以增加能量消耗,防止饮食引起的肥胖。
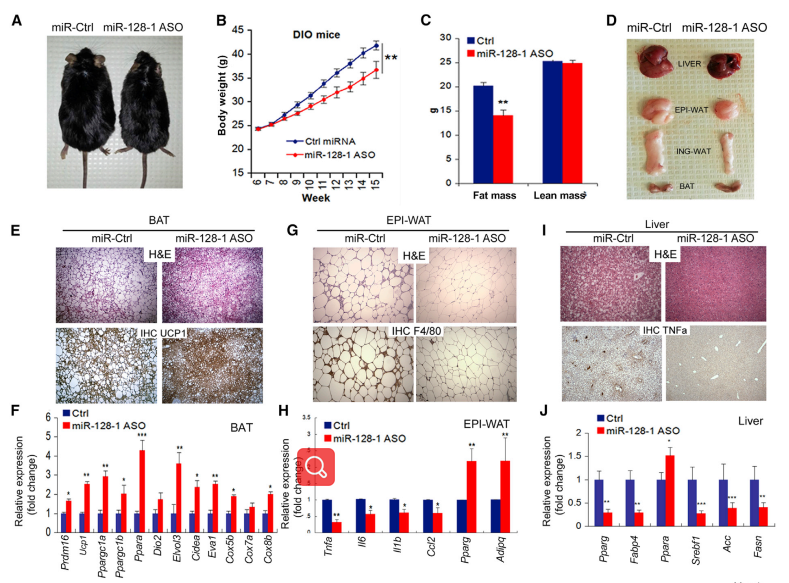
图一:miR-128-1 ASO抑制miR-128-1,可预防饮食诱导的肥胖,减少脂肪细胞肥大和炎症,预防肝脏脂肪变性和炎症,增加全身能量消耗,改善葡萄糖稳态
肥胖和肝脏和骨骼肌的异位脂肪沉积通常与胰岛素抵抗和葡萄糖控制不良有关,是T2D发病的主要危险因素。DIO小鼠高血糖,中度胰岛素抵抗; 葡萄糖和胰岛素耐量试验显示,anti-miR-128-1治疗可显著改善这些异常代谢特征。为了进一步确定miR-128-1在肥胖相关血糖异常中的作用,作者对anti-miR-128-1治疗和anti-miR对照的DIO小鼠进行了高胰岛素-降血糖钳夹研究。结果发现,miR-128-1是葡萄糖稳态和胰岛素敏感性的关键调节因子。接下来,作者还评估了miR-128-1是否也可能导致经典瘦素缺乏ob/ob遗传肥胖小鼠模型的代谢异常。最终得出结论,即miR-128-1是整个动物代谢的重要调节器,作为一种节俭的miRNA,通过在多种代谢组织(如WAT、BAT、肝脏和骨骼肌)中的明显作用,抑制能量消耗。
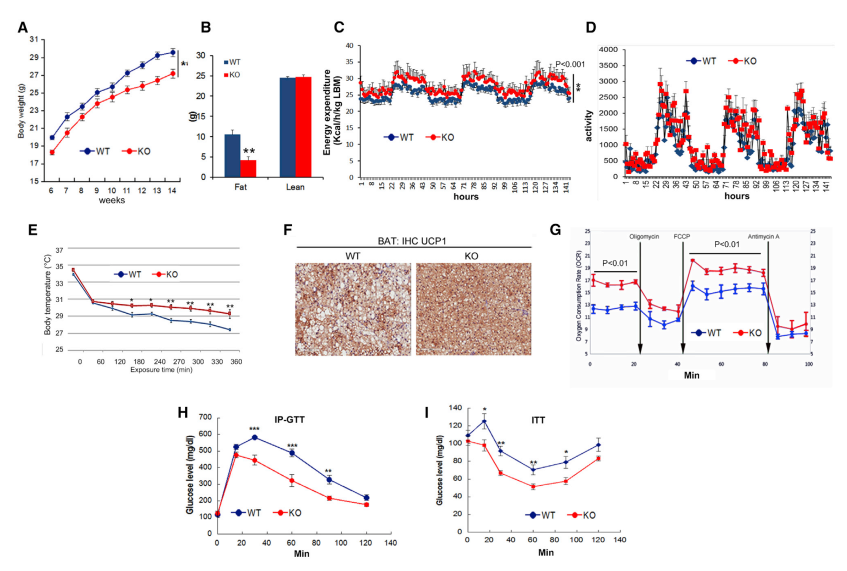
图二:miR-128-1缺乏可预防肥胖,增加全身能量消耗,改善葡萄糖稳态
总结
综上所述,数据显示,miR-128-1在从能量消耗到能量储存的代谢转换过程中发挥了关键作用,而miR-128-1基因组位点与正选择和异常代谢的联系补充了LP在该位点的作用。的确,在古代,miR-128-1表达的改变可能是有益的,但现在,由于持续的热量丰富,可能构成代谢失调,易导致肥胖和T2D。因此,miR-128-1可能是治疗代谢性疾病如肥胖和T2D的治疗靶点。
原文链接
https://doi.org/10.1016/j.cell.2020.09.017
参考文献
1.Ahfeldt, T., Schinzel, R.T., Lee, Y.K., Hendrickson, D., Kaplan, A., Lum, D.H., Camahort, R., Xia, F., Shay, J., Rhee, E.P., et al. (2012). Programming human pluripotent stem cells into white and brown adipocytes. Nat. Cell Biol. 14, 209–219.













