白细胞介素37b(以下称为IL-37)被确定为天然和获得性免疫的基本抑制剂。IL-37 在结直肠癌 (CRC) 中的分子机制和功能一直难以捉摸。
2022年1月20日,四川大学李炯及藤秀共同通讯在在Signal Transduction and Targeted Therapy (IF=18)在线发表题为“Interleukin-37 promotes colitis-associated carcinogenesis via SIGIRR-mediated cytotoxic T cells dysfunction”的研究论文,该研究发现 IL-37 转基因 (IL-37tg) 小鼠对结肠炎相关的结直肠癌 (CAC) 高度敏感,并且结肠肿瘤负担显著增加。然而,IL-37 对于肠道诱变、CRC 细胞增殖、凋亡和迁移是可有可无的。值得注意的是,IL-37 在 CAC 和 B16-OVA 模型中抑制了保护性细胞毒性 T 细胞介导的免疫。
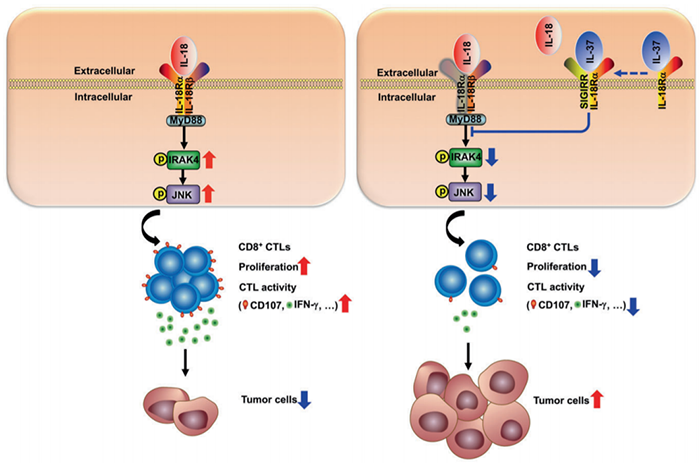
IL-37 导致的功能障碍拮抗 IL-18 诱导的CD8+ T 细胞增殖和效应功能,这依赖于 SIGIRR(单一免疫球蛋白白细胞介素 1 受体相关蛋白)。最后,该研究观察到 CRC 患者的 IL-37 水平显著升高,与血清 CRC 生物标志物 CEA 水平呈正相关,但与 CRC 患者的 CD8+ T 细胞浸润呈负相关。总之,该研究结果强调了 IL-37 在通过灭活细胞毒性 T 细胞来利用抗肿瘤免疫中的作用,并在癌症免疫周期中建立了一个新定义的抑制因子 IL-37/SIGIRR 作为 CRC 的治疗靶点。

结直肠癌是全球发病率和死亡率的主要原因。CD8+ 细胞毒性 T 淋巴细胞 (CTL) 是攻击癌症的首要免疫细胞。一些研究已经确定了肿瘤和侵袭性边缘的 CD8+ CTLs 密度以评估 CRC 的复发风险。CD8+ CTL 浸润可以作为 CRC 患者良好生存结果的独立预测因子。CD8+ CTL 浸润对免疫检查点阻滞剂的反应率很高。这些发现表明 CD8+ CTL 是 CRC 的关键防御者。 CD8+ CTLs 主要通过 IFN-γ 介导或穿孔素介导的机制杀死肿瘤细胞。IFN-γ 作为一种 CD8+ CTL 衍生的细胞毒性细胞因子,可以通过激活 JAK-STAT1-caspase3 级联来启动肿瘤细胞的凋亡。穿孔素介导的肿瘤杀伤机制是通过CD8+ CTLs的脱颗粒实现的,例如释放脱颗粒的货物,包括细胞毒性蛋白穿孔素和颗粒酶。穿孔素促进跨膜孔的形成,导致颗粒酶进入肿瘤细胞并引发细胞凋亡。细胞因子作为分泌蛋白,可以为免疫细胞提供关键线索,因此它们是癌症免疫治疗的有吸引力的候选靶点。IL-18 是 IL-1 家族的成员,通过由 IL-18Rα 和 IL-18Rβ 亚基组成的异二聚体受体驱动 MyD88–IRAK4–JNK 信号传导。先前的研究报告称,IL-18 与 IL-12 协同作用可刺激 CD8+ T 细胞中细胞毒性细胞因子 IFN-γ 的产生。先前已观察到重组 IL-18 在 CRC 的临床前模型中抑制肿瘤进展。此外,重组 IL-18 作为抗癌药物在临床试验中具有良好的安全性和良好的耐受性。这些发现重新定义了 IL-18 作为一种抗肿瘤细胞因子的关键作用,它从根本上改变了免疫肿瘤微环境。白细胞介素37(IL-37)是一种新的IL-1家族成员,作为最近发现的IL-18抑制因子,在肾小管上皮细胞中干扰IL-18依赖性炎症因子(TNF-α、IL-1β 和 IL-6)的表达。先前的研究证明,由 IL-37、SIGIRR 和 IL-18Ra 组成的三方复合物对于 IL-37的功能是必不可少的。SIGIRR 是一种孤儿受体,SIGIRR 的过表达抑制Jurkat 和 HepG2 细胞中的 IL-18 信号传导。这些发现表明 SIGIRR 可能在 IL-37 抑制 IL-18 信号传导方面发挥关键作用。IL-37 监测自然免疫,并作为获得性免疫的关键调节分子出现。文章模式图(图源自Signal Transduction and Targeted Therapy )IL-37 减弱了 Th1 反应,但促进了 ConA 中 Th2 细胞因子(IL-13 和 IL-4)的产生,从而导致肝损伤。IL-37 刺激提高了患有传染病和过敏症的受试者的 Tregs 细胞比例。这些发现表明 IL-37 是 T 细胞免疫反应的重要调节因子。考虑到 IL-37 的抗炎特性,已经发现 IL-37 可以影响一些癌症的发展,例如非小细胞肺癌、肝细胞癌、宫颈癌和结肠癌。然而,IL-37的免疫学作用和功能机制在肿瘤微环境中仍然难以捉摸。具体而言,IL-37 对 CD8+ CTL 肿瘤免疫监视的作用尚不清楚。发现和理解关键分子和生物过程将为开发有效的癌症疗法提供宝贵的指导。许多 IL-1 家族成员在抗肿瘤免疫反应中表现出至关重要的调节作用,从而影响肿瘤免疫逃逸。新型 IL-1 家族成员 IL-37 在肿瘤微环境中的功能机制尚不清楚。在这里,该研究证实抗炎细胞因子 IL-37 可以作为功能失调的细胞毒性 CD8+ T 细胞的关键诱导剂,从而促进结肠炎相关的癌变。此外,该研究表明,IL-37 通过其抑制性受体 SIGIRR 拮抗 IL-18 诱导的 CD8+ T 细胞的细胞毒活性。这些发现增强了对肿瘤微环境中 IL-1 家族的认识,突出了 IL-37 在利用抗肿瘤免疫中的作用。此外,癌症免疫周期中新定义的抑制因子 IL-37/SIGIRR 被确立为结直肠癌的治疗靶点。 https://www.nature.com/articles/s41392-021-00820-z