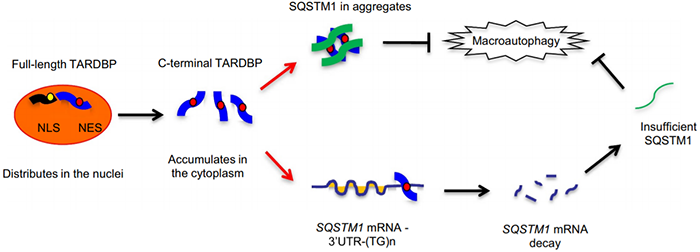
TARDBP/TDP-43(TAR DNA 结合蛋白)的细胞质积累和聚集是肌萎缩侧索硬化和额颞叶变性的病理标志。TARDBP 的灵长类动物特异性切割解释了其在灵长类动物大脑中的细胞质错误定位,但细胞质 TARDBP 如何介导神经病理学,不是很清楚。
2021年12月22日,暨南大学李晓江,李世华及殷鹏共同通讯在Autophagy (IF=16)在线发表课题组题为“SQSTM1-mediated clearance of cytoplasmic mutant TARDBP/TDP-43 in the monkey brain”的研究论文,该研究报道了细胞质突变体 TARDBP 通过与灵长类动物 SQSTM1 转录本的独特 3'UTR 序列 (GU/UG)n 结合,诱导 SQSTM1 mRNA 不稳定性,从而选择性地降低猴脑中的 SQSTM1 表达。SQSTM1 的过表达可以通过增强巨自噬/自噬活性来减少猴脑中细胞质 C 末端 TARDBP 的积累。
总之,该研究结果为细胞质 TARDBP 的发病机制和突变 TARDBP 介导的神经病理学的潜在疗法提供了额外的线索。
TARDBP/TDP-43(TAR DNA 结合蛋白)在肌萎缩侧索硬化症 (ALS)、额颞叶变性 (FTLD)和其他神经系统疾病患者的大脑中形成聚集体。TARDBP 中两个保守的 RNA 识别基序 RRM1 和 RRM2 赋予其核酸结合活性以调节基因转录或 RNA 加工的不同功能。通过在低纳摩尔范围内结合对富含 UG 的保守序列具有高特异性的单链 RNA,TARDBP 被募集到剪接位点以抑制外显子识别 或 mRNA 不稳定性。TARDBP 还与 3'-非翻译区 (3'- UTR) 介导 mRNA 的降解,甚至是其自身的 mRNA,以抑制基因表达。因此,TARDBP的病理积累可导致基因表达异常。众所周知,大部分导致 FTD-ALS 的基因直接或间接与通过巨自噬/自噬维持蛋白质稳态的途径相关,并涉及诸如 UBQLN2(泛素 2)、OPTN(optineurin)、VCPVCP (valosin containing protein) 和 SQSTM1(sequestosome 1)。在这些蛋白质中,SQSTM1 是 N 端规则通路的 N 识别素,可调节自噬体生物发生。SQSTM1 基因的突变首先在Paget病中发现,最近在 ALS 和 FTLD 患者中发现。SQSTM1 参与 ALS 和 FTLD 的证据还包括患者大脑中存在 SQSTM1 阳性包涵体,这导致蛋白酶体和自噬的抑制以及有毒蛋白质的积累。然而,ALS 和 FTLD 相关的 SQSTM1 变异在疾病发作和进展中的作用仍不清楚。目前对 SQSTM1 相关发病机制的理解主要基于培养的细胞或小动物模型。敲除 sqstm1 的小鼠表现出过度磷酸化 MAPT/tau 的积累增加和随后的神经变性,而 SQSTM1 的缺失导致运动神经元变性增加、SNCA/α-突触核蛋白病理学增强和加剧了小鼠的运动表型和神经病理学结果。SQSTM1 在灵长类动物大脑中清除细胞质突变体 TARDBP 的作用的拟议模型(图源自Autophagy )尽管小鼠模型为重要的病理事件和机制见解提供了有价值的信息,但物种差异阻止了小动物重现患者大脑中看到的一些重要病理变化。例如,与显示明显细胞质 TARDBP 包涵体 的 ALS 患者大脑相比,大多数 ALS 转基因啮齿动物模型显示突变 TARDBP的主要核定位或细胞质 TARDBP。然而,在转基因突变型 TARDBP 猪模型和表达突变型 TARDBP的猴脑中,TARDBP 定位于细胞质中形成具有病理特征的聚集体,包括高度泛素化、磷酸化和切割的 TARDBP 形式,它们是类似于在患者大脑中看到的。此外,在小鼠中未发现人类特异性 TARDBP 错接。尽管在细胞培养物中观察到有毒的功能获得效应,但灵长类动物大脑中细胞质 TARDBP 的影响仍有待充分研究。因为突变的 TARDBP 在大型动物的大脑中积累在细胞质中,并且因为非人类灵长类动物更接近人类,该研究探索了细胞质突变 TARDBP 在猴脑中的影响。研究结果表明,细胞质突变 TARDBP 通过影响 SQSTM1 的表达来损害自噬功能,而过表达 SQSTM1 可以通过促进自噬功能来减少细胞质 TARDBP 聚集体的积累。该研究结果为 TARDBP 相关神经系统疾病的发病机制和潜在治疗提供了额外的线索。论文第一作者及通讯作者为暨南大学殷鹏研究员,暨南大学郭祥玉、李邦副研究员等也参与了本项目的研究。暨南大学附属第一医院影像中心王璐研究员为猴影像学观察做出了重要贡献。暨南大学李世华教授和李晓江教授为文章的共同通讯作者。本研究获得广东省科技厅项目,科技部国家重点研发计划,国家自然科学基金及广东省非人灵长类动物模型研究重点实验室平台的资助。https://www.tandfonline.com/doi/full/10.1080/15548627.2021.2013653