最新在中心上线的发表在Cell Press细胞出版社旗下期刊Cell上,名为"Genome-wide CRISPR screens reveal host factors critical for SARS-CoV-2 infection"的研究,来自耶鲁大学医学院的研究团队进行了全基因组范围内的CRISPR筛选,通过敲除每一个宿主因子来研究病毒的宿主因子,是一项十分全面的宿主病毒相互作用机制的研究。
*以下中文内容仅供参考,请以英文原文为准。
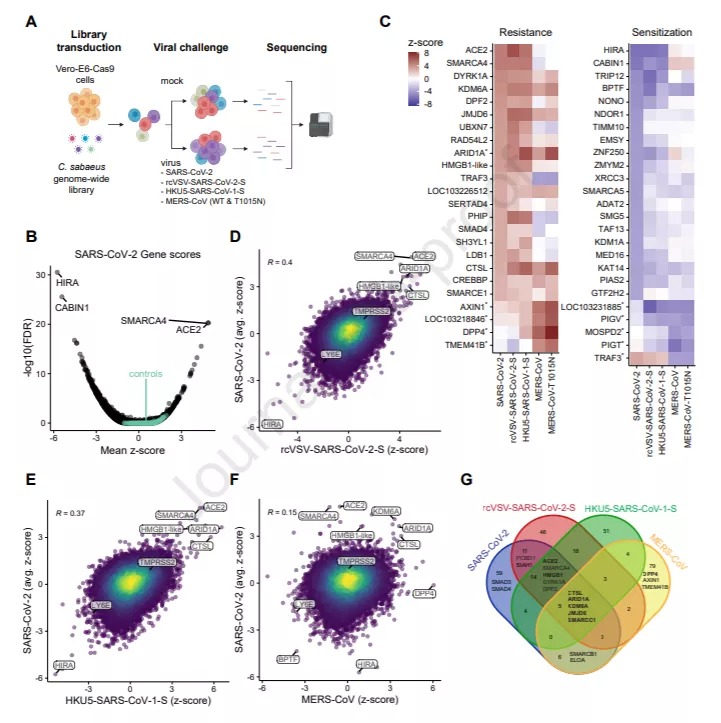
摘要 鉴定对SARS-CoV-2感染至关重要的宿主基因或有望揭示新的治疗靶点,并有助于我们了解COVID-19的发病机制。在此,我们对SARS-CoV-2、MERS-CoV、表达SARS-CoV-1刺突蛋白的蝙蝠冠状病毒HKU5,以及VSV感染的表达SARS-CoV-2刺突蛋白的Vero-E6细胞中进行了全基因组CRISPR筛查。我们确定了已知的SARS-CoV-2宿主因子,包括受体ACE2和组织蛋白酶L。我们还发现了具有促病毒(pro-viral)作用的基因和通路,包括HMGB1与SWI/SNF组成的染色质重塑复合体,它们分别具有SARS谱系特异性和泛冠状病毒特异性。本研究显示,HMGB1调节ACE2表达,对于SARS-CoV-2、SARS-CoV-1和NL63的病毒进入至关重要。我们的研究还显示,针对已鉴定的基因产物的小分子拮抗剂抑制了猴和人类细胞中的SARS-CoV-2感染,从而证明了这些基因突变在物种间的保守性。这些结果共同确定了SARS-CoV-2的潜在治疗靶点,并揭示了SARS谱系特异性和泛冠状病毒特异性的宿主因子,这些因子可调节对高致病性冠状病毒的易感性。 简介 病毒进入是冠状病毒生命周期的第一阶段,由病毒刺突蛋白所介导。刺突蛋白的受体结合结构域与特定的细胞表面受体结合,后者是决定受感染宿主多样性和细胞向性的主要因素(Letko, Marzi and Munster, 2020; Shang et al., 2020)。SARS-CoV-1、SARS-CoV-2和NL63使用血管紧张素转换酶2(ACE2),而MERS-CoV使用二肽基肽酶4(DPP4)作为受体(Li et al., 2003; Hofmann et al., 2005; Raj et al., 2013; Letko, Marzi and Munster, 2020)。冠状病毒刺突蛋白在进入细胞前需要经过两个蛋白水解处理步骤。第一次水解事件可以发生在生产者细胞内、细胞外环境或内体中,而且可以由包括弗林蛋白酶和TMPRSS2在内的几种蛋白酶所介导(Hoffman, Kleine-Weber and Pöhlmann, 2020; Walls et al., 2020;Yan et al., 2020; Zang et al., 2020)。暴露病毒融合肽的第二次蛋白水解事件可以由TMPRSS2介导发生在靶细胞质膜上,或者由组织蛋白酶L介导发生在内体中(Hoffmann et al., 2020; Ou et al., 2020)。在病毒膜融合后,病毒RNA被释放至细胞质中,经过转录、翻译,并且在组装和出芽分泌之前完成病毒复制和转录复合体的形成(Snijder et al., 2006; Stertz et al., 2007; Knoops et al., 2008)。然而,我们目前尚不清楚介导这些过程的宿主基因。 鉴定对感染至关重要的宿主因子对于了解冠状病毒的发病机理,揭示宿主的易感性差异,以及开发针对宿主的新型疗法至关重要,这些疗法可能具有抗击当前和未来冠状病毒大流行的效果。为了揭示SARS-CoV-2感染和细胞死亡所必需的宿主基因,我们在绿猴(非洲绿猴或黑尾猴)Vero-E6细胞系中对SARS-CoV-2、SARS-CoV-1和MERS-CoV进行了全基因组CRISPR筛查。 Vero-E6细胞在SARS谱系和MERS-CoV基因筛查中具有多种独特的优势。首先,Vero-E6细胞和非洲绿猴对SARS谱系(SARS-CoV-1和SARS-CoV-2)和MERS-CoV均敏感,因此可以对所有三种高致病性冠状病毒进行直接比较(Clay et al., 2012; Matsuyama et al., 2020; Ogando et al., 2020; Totura et al., 2020; Woolsey et al., 2020)。其次,Vero-E6细胞内源性表达ACE2和DPP4,这使得我们能够发现新的受体表达调节剂。如果是在外源性启动子下过表达ACE2或DPP4的转基因细胞系,这也许是不可能的(Heaton et al., 2020)。重要的是,吸烟既上调ACE2表达,又是重症COVID-19的危险因素,突显了揭示ACE2调节决定因素的重要性(Smith et al., 2020)。第三,与其他易感染冠状病毒的细胞系(例如Huh7.5)不同,Vero-E6细胞感染SARS谱系和MERS-CoV后具有更多的细胞病变性,因此能够在病毒生命周期的后期进行筛选,而不是根据病毒编码蛋白或报告基因的表达进行筛选。值得注意的是,Vero-E6细胞不表达I型干扰素。尽管这可能会妨碍某些基因的识别,但它提供了一种简化系统,可以减少对干扰素刺激基因的潜在偏差(Desmyter, Melnick and Rawls, 1968; Emeny and Morgan, 1979; Chew et al., 2009)。 本研究中,我们使用了C. sabaeus全基因组汇总的CRISPR文库,该文库由83,963个靶向单向导RNA(sgRNAs)所组成,每个基因平均包含四个sgRNAs,以及1,000个非靶向对照sgRNA。我们最初利用了表达两种不同Cas9核酸酶构建体(Cas9-v1和Cas9-v2)的Vero-E6细胞系进行了两次独立的SARS-CoV-2全基因组筛选。Cas9-v2具有额外的核定位序列,可增强其活性。然后,我们用C. sabaeus sgRNA文库转导了上述两种Vero-Cas9细胞系,并用SARS-CoV-2攻击了细胞(图1A)。SARS-CoV-2筛查确定了许多基因,这些基因在被sgRNA靶向时具有抗性(前病毒)或致敏性(抗病毒),与非靶向sgRNA相比具有显著的差异性(图1B-C),表明了筛查的高技术质量。 ▲图1 我们的筛查确定了针对SARS谱系和MERS-CoV的蛋白酶组织蛋白酶L,以及分别针对SARS谱系病毒和MERS-CoV的病毒受体ACE2和DPP4。我们确定了SARS-CoV-2特异性、MERS-CoV特异性和泛冠状病毒特异性的基因,并发现调节SARS-CoV-2感染的大多数基因都在病毒进入水平起作用。我们对顶层CRISPR命中基因进行了汇总和单独验证。具体来说,我们确定了HMGB1和SWI/SNF染色质重塑复合物是促病毒进入的。我们还发现HMGB1对于ACE2表达和SARS-CoV-1、SARS-CoV-2和NL63的细胞进入至关重要,所有这些病毒都使用ACE2作为受体。相比之下,几种SWI/SNF复合体对于SARS谱系和MERS-CoV的细胞入侵都至关重要,但对甲型流感病毒(IAV)或脑心肌炎病毒(EMCV)并不是必需的,这表明了冠状病毒的特异性。另外,我们证明了促病毒基因产物的小分子拮抗剂在体外可抑制SARS-CoV-2感染Vero-E6细胞和人类细胞。这些命中基因代表了SARS-CoV-2的新型治疗靶点,也加深了我们对COVID-19发病机制的了解。 讨论 我们对影响大流行性冠状病毒SARS-CoV-2和MERS-CoV以及重组蝙蝠冠状病毒HKU5-SARS-CoV-1-S感染的宿主基因进行了全基因组筛查。对病毒受体ACE2和DPP4以及蛋白酶CTSL的成功鉴定证明了筛查的技术质量,使人们对筛查调节SARS-CoV-2感染的其他基因充满了信心(Hoffmann et al., 2019, 2020; Ou et al., 2020; Shang et al., 2020)。我们发现了涉及多种生物过程的基因,包括染色质重塑、组蛋白修饰、细胞信号转导和RNA调控过程。我们以汇总分析和阵列分析方式验证了关键基因,包括促病毒和抗病毒基因,并确定了一些小分子拮抗剂,这些拮抗剂可以保护Vero-E6细胞、人类肝细胞和人类肺细胞免受SARS-CoV-2诱导产生的死亡和感染。 我们的筛查确定了许多在染色质调节和组蛋白修饰中具有功能性作用的基因,这些基因突显了表观遗传调节致病性冠状病毒感染的潜在重要性。既往研究发现,在MERS-CoV和SARS-CoV-1感染后,表观遗传过程参与调节抗原呈递和干扰素刺激的基因诱导(Menachery et al., 2014, 2018; Schäfer and Baric, 2017);但是,鉴于Vero-E6细胞不表达I型干扰素,这些过程可能具有不同的作用机制。有趣的是,大多数促病毒和抗病毒基因在都在病毒进入水平发挥作用,而且这一结果在SARS-CoV-2和rcVSV-SARS-CoV-2-S筛查之间具有高度一致性。我们确定了调节冠状病毒进入的ACE2依赖性机制和独立机制。 具体来说,我们发现HMGB1在调节ACE2表达方面以及因此对SARS-CoV-1、SARS-CoV-2和NL63具有易感性的新型表观遗传学作用。我们在Vero-E6细胞和两种IFN充分表达的人类细胞系中都证明了这一点。HMGB1是一种多效性蛋白,可结合调节核内染色质的核小体,充当非自体核酸的“前哨卫兵”,转运遗传物质;并在应对病毒感染时充当警报蛋白,分泌至细胞外(Menachery et al., 2014; Andersson, Ottestad and Tracey, 2020; Simpson et al., 2020)。值得注意的是,在动物模型中,抗HMGB1疗法可以减少呼吸道合胞病毒复制和IAV诱导的肺部疾病(Manti et al., 2018; Hatayama et al., 2019),而在腺病毒感染中,病毒蛋白VII会结合HMGB1并抑制其促炎功能(Avgousti et al., 2016)。另外值得注意的是,我们发现HMGB1以细胞固有的方式调节ACE2的表达,而不是以其作为细胞因子或警报蛋白的功能进行调节,表明了HMGB1在SARS-CoV-2感染中的独特机制。 经过鉴定,我们发现编码SWI/SNF染色质重塑复合物成分的基因是SARS-CoV-2、MERS-CoV和HKU5-SARS-CoV-1-S的促病毒基因,这表明该复合物对致病性冠状病毒具有广泛的重要性。而且我们还发现这些基因也是rcVSV-SARS-CoV-2-S的促病毒基因,提示SWI/SNF复合体在促进冠状病毒进入中也发挥了一定的作用。SWI/SNF复合物的组成包括催化性ATPase亚基(SMARCA2或SMARCA4),以及更大的非催化性蛋白支架核心,该核心蛋白通过ARID1A与ATPase桥接(Mashtalir et al., 2018)。SWI/SNF复合物缺乏固有的DNA序列特异性,因此其靶向特异性是由DNA结合蛋白赋予的,DNA结合蛋白结合这一复合物并将其募集到基因组的靶定位点,然后在此处滑动并弹出核小体,从而调节染色质的可及性和基因表达。我们推测SWI/SNF复合物的促病毒作用可能受到了组蛋白H3.3(HUCA伴侣)复合物的拮抗。经证明,组蛋白H3.3(HUCA伴侣)复合物与SWI/SNF复合物共同作用于染色质(Pchelintsev et al., 2013)。 本研究发现的促病毒和抗病毒基因对于我们理解COVID-19的发病机理、治疗方法和疫苗设计具有重要意义。首先,SARS-CoV-2可以引起多种疾病严重程度的表型,从无症状感染到严重的呼吸衰竭和死亡(Wang et al., 2020; Zhu et al., 2020)。我们尚不清楚人与物种之间存在疾病严重程度差异的基础。由于疾病易感性可能与抗性基因的表达呈正相关,而在细胞、组织和机体水平上与致敏性基因呈负相关,因此本研究发现的基因和通路可以解释这种变化。例如,吸烟既增加了ACE2的表达,又加剧了COVID-19的致病性(Smith et al., 2020)。潜在的调控网络是未知的,但是非常有趣的是,我们推测此处发现的染色质和组蛋白修饰基因有助于表达复杂多样的促病毒基因表达程序,该程序或许能调节ACE2和其他介导病毒相互作用的基因。此外,尽管Vero-E6细胞缺乏干扰素,我们仍然发现干扰素刺激基因LY6E是SARS谱系和MERS-CoV的抗病毒进入因子。这表明在缺乏I型干扰素的情况下,LY6E仍有基础表达。最近的一项研究确定了Ly6E是一种泛冠状病毒的抗病毒分子(Pfaender et al., 2020),本研究报道的结果与之一致,并揭示了Vero-E6细胞可作为揭示致病性冠状病毒宿主-病原体相互作用的模型系统,具有相当的实用性和适用性。 ▌论文标题: Genome-wide CRISPR screens reveal host factors critical for SARS-CoV-2 infection ▌论文网址: https://www.cell.com/cell/fulltext/S0092-8674(20)31392-1#%20 ▌DOI: https://doi.org/10.1016/j.cell.2020.10.028