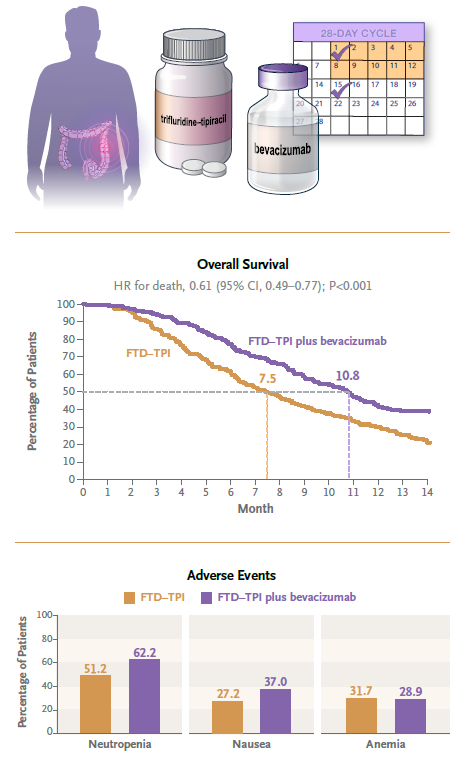
目前,曲氟尿苷-替吡嘧啶(Trifluridine-Tipiracil,FTD-TPI)在治疗难治转移性结直肠癌过程中,已经被广泛用作三线或者四线治疗手段。而为了更进一步延长患者的总生存期,初步的临床II期数据表明FTD-TPI联合贝伐珠单抗(Bevacizumab)有很大的潜力可以延长总生存期。近日,来自西班牙巴塞罗那瓦尔德西布伦大学医院和肿瘤研究所(Vall d’Hebron Hospital Campus and Institute of Oncology)的Josep Tabernero教授在国际医学期刊《新英格兰医学杂志》(NEJM)杂志上发表了文章:Trifluridine-Tipiracil and Bevacizumab in Refractory Metastatic Colorectal Cancer。本临床III期SUNLIGHT研究结果显示FTD-TPI联合Bevacizumab治疗的中位总生存期(mOS)和中位无进展生存期(mPFS)分别为10.8个月和5.6个月;而FTD-TPI单药治疗的mOS和mPFS分别为7.5个月和2.4个月;并且联合治疗组和单药治疗组的不良反应无显著差异。本试验受试者入选标准如下:受试者需满足18岁及以上并且各器官功能相对完整,美国东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)表现状态评分为0或者1(该评分范围为0-5,评分越高代表健康程度和活动能力越差)。组织学确诊、不可切除的结直肠或结肠腺癌患者既往接受不超过两种晚期结直肠癌化疗方案,并且疾病进展,或者上一种化疗方案引起了不可接受的不良反应。既往治疗必须包括氟嘧啶、伊立替康、奥沙利铂、抗VEGF单克隆抗体(不一定是Bevacizumab)或抗EGFR单克隆抗体(用于RAS野生型疾病受试者),如果疾病在治疗期间或最后一次新辅助或辅助治疗后6个月内复发,治疗可以包括新辅助或辅助化疗。入组的受试者将以1∶1的比例随机分组,分别接受FTD-TPI 联合Bevacizumab治疗或FTD-TPI单独治疗。FTD-TPI在每28日的第1~5日和第8~12日口服给药,每日2次,起始剂量为35 mg/m2。Bevacizumab剂量为5 mg/kg,在第1日和第15日静脉给药。本临床试验的主要终点是总生存期(OS);次要终点包括研究者判定的无进展生存期(PFS),客观缓解率(ORR)和疾病控制率(DCR)等。共计492名受试者入组本临床试验(每组各246名)。经过约14个月的随访期统计显示:FTD-TPI联合Bevacizumab治疗的中位总生存期(mOS)和中位无进展生存期(mPFS)分别为10.8个月和5.6个月;而FTD-TPI单药治疗的mOS和mPFS分别为7.5个月和2.4个月。两组中最常见的不良事件是中性粒细胞减少症、恶心和贫血,且无显著差异;同时也没有治疗相关的死亡报告发生。此外,FTD-TPI联合Bevacizumab治疗组中ECOG表现状态评分从0或1分恶化到2分以上的中位时间为9.3个月,而FTD-TPI单药治疗组为6.3个月。总体来说,本临床III期SUNLIGHT研究说明FTD-TPI联合Bevacizumab治疗可以更加延长患者的总生存期。Gerald W. Prager博士和Julien Taieb博士为本文的共同第一作者,Josep Tabernero教授为通讯作者。本SUNLIGHT临床研究由Servier 和Taiho Oncology公司资助完成。
原文链接:https://doi.org/10.1056/NEJMoa2214963
NEJM主编针对原文评述链接:https://doi.org/10.1056/NEJMe2300385