要说生命科学领域单个分子撑起一个领域的,p53说第二,没有其他分子敢说第一。差不多20年前,笔者第一次听到p53的大名。想不到时至今日,p53仍然是生命科学领域的研究热点。笔者在PubMed上以p53为关键词检索了一下历年的相关论文,发现关于p53的总论文数已经超过10万篇了。而且,近10年来,年发文量就从未低于5000篇,其热度可见一斑。
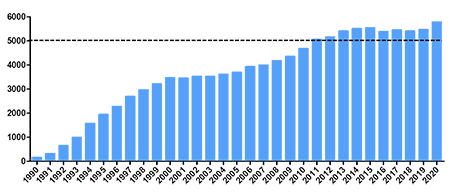
p53作为生物体内著名的抑癌基因,主要作为转录因子调节一系列基因的转录,从而发挥作用。就目前的研究而言,p53的功能几乎参与调控所有的生物学过程,包括细胞凋亡,细胞周期,细胞衰老,细胞分化,细胞迁移,细胞代谢和细胞自噬等等。
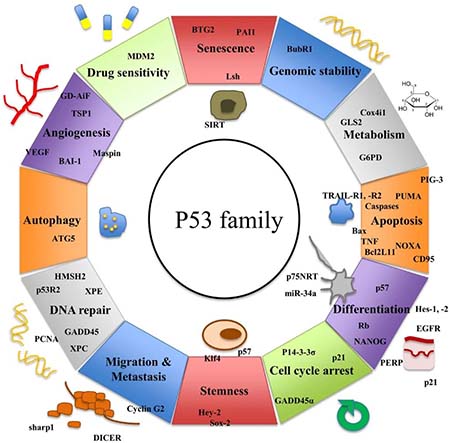
令人惊奇的是,当p53基因发生突变后,由于空间构象变化,不仅使得p53失去了抑癌功能,而且突变本身甚至会赋予p53癌基因的功能。目前,围绕突变型p53展开的研究是p53领域的一大热点研究方向。
在今年4月份发表于Cancer Cell(2020 IF: 31.743)的一篇论文中,研究者发现突变型p53通过抑制先天免疫信号通路促进肿瘤的发生。该项研究为突变型p53的促癌作用提供了全新的分子机制。论文发表后,受到了《Science Signaling》等杂志的专文推介。该项研究绝对称得上近年来p53领域的重磅研究发现之一。
标题
Mutant p53 suppresses innate immune signaling to promote tumorigenesis

文献解读
突变型p53抑制先天免疫信号通路
先天免疫通路是机体防御外来病原体感染的第一道防线,DNA受体通路是先天免疫通路的重要分支。DNA受体通路通过感应细胞中自身或者入侵病原菌来源的DNA,诱导I型干扰素和炎性细胞因子的产生,激活机体的先天免疫反应。cGAS-STING通路是近年来鉴定出来的最为重要的DNA受体通路之一。cGAS通过结合自身损伤的DNA或者外源病原体DNA,合成第二信使cGAMP,cGAMP与内质网定位的接头蛋白STING结合并活化STING,进一步激活TBK1,诱导转录因子IRF3和NF-kB入核,产生I型干扰素和炎性细胞因子。
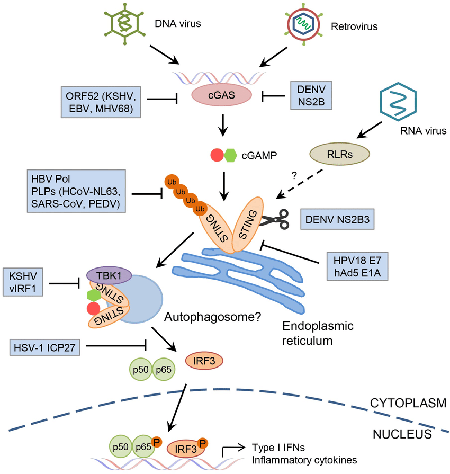
在本项研究中,研究者发现在表达突变型p53的细胞内敲低/敲除p53均会激活cGAS-STING通路。有意思的是,在表达野生型p53的细胞(A549)内敲低p53,则会抑制cGAS-STING通路。换句话说,野生型p53与突变型p53在cGAS-STING通路中发挥完全相反的作用。
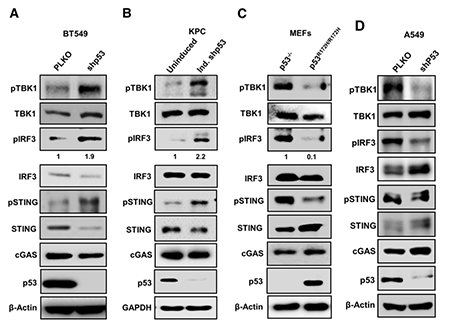
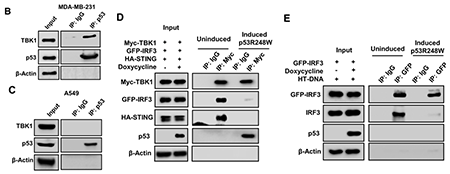
突变型p53抑制TBK1-STING-IRF3三元复合物的形成
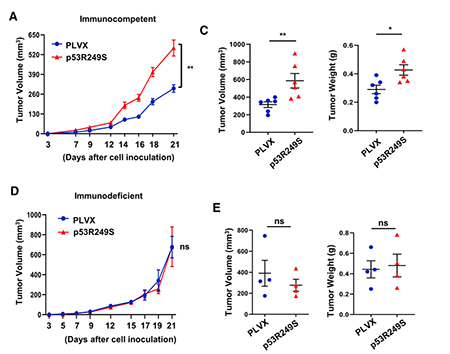
突变型p53的促癌作用依赖于机体免疫系统
搞清楚了分子机制后,研究者返回到肿瘤研究中继续探究突变型p53的可能作用。他们发现,在免疫系统功能完好的小鼠模型中,突变型p53能够显著促进肿瘤的生长;而在免疫系统功能缺失的小鼠模型中,突变型p53则无法进一步促进肿瘤的生长。以上结果表明,突变型p53的促癌作用可能依赖于对机体免疫功能的某种调控。
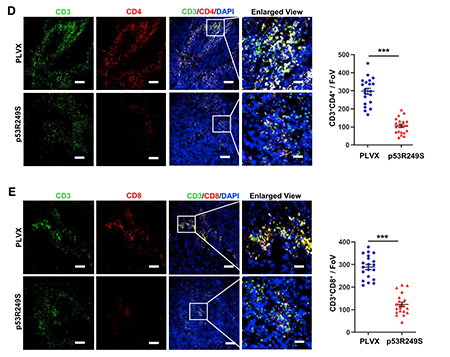
突变型p53抑制机体的免疫监视功能
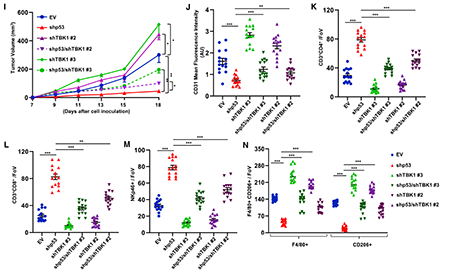
研究者发现,如果在表达突变型p53的肿瘤组织中敲低p53,肿瘤的生长受到显著抑制,肿瘤微环境中的免疫细胞的数量也会得到显著提高。有意思的是,在敲低突变型p53的基础上进一步敲低TBK1,肿瘤的生长抑制则会完全解除,肿瘤微环境中的免疫细胞的数量也会显著下降。也就是说,突变型p53对机体免疫功能的抑制作用主要依赖于TBK1代表的先天免疫通路。
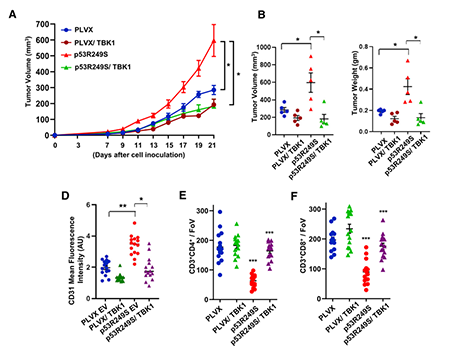
高表达TBK1能够完全消除突变型p53对肿瘤生长的促进作用
基于以上发现,研究者推测,如果在肿瘤组织中恢复TBK1的活性可能能够对抗突变型p53的促肿瘤作用。不出所料,在表达突变型p53的肿瘤组织中过表达TBK1能够显著减缓肿瘤的生长速度。此外,肿瘤微环境中的免疫细胞数量也得到了显著回升。
以上研究结果表明,在表达突变型p53的肿瘤类型中,靶向激活TBK1可能会产生不错的治疗效果。
总结而言,该项研究发现了“老”分子p53的“新”功能,即突变型p53在当下无比火热的肿瘤免疫中发挥负向调控作用。该项研究是近年来p53领域屈指可数的亮点发现之一,极大地拓宽了学术界对p53的认识,同时也为突变型p53相关的肿瘤类型提供了全新的潜在治疗靶点。
文章来源:解螺旋
参考文献:
Ghosh, M. et al. Mutant p53 suppresses innate immune signaling to promote tumorigenesis. Cancer cell, 2021, 39, 494-508 e495.













