肺癌是人类肿瘤的头号杀手。虽然近年来靶向治疗和免疫治疗取得了突破性进展,但患者仍会出现耐药、免疫治疗无效等情况。在单细胞水平上研究可以精确了解患者体内、以及患者间的异质性,提高细胞差异性研究的分辨率,帮助更好指导治疗。
背景介绍

数据介绍
单细胞测序数据(10x Genomics):
入组5例未经治疗的NSCLC患者,其中2例腺癌,2例鳞癌,1例大细胞癌。采集每例患者的3份肿瘤组织样本、以及1份同一肺叶下远端正常肺组织样本,进行单细胞测序。
入组3例未经治疗的NSCLC患者作为验证集。
外部数据
TCGA数据库以及其它研究中的1572名NSCLC RNA-Seq数据及预后信息 (1027 LUAD 和 545 LUSC)。
结果分析
结果解析
共获得了52,698个细胞,其中有39,323细胞来源于肿瘤; 13,375个来源于正常组织。
52,698个细胞中覆盖了约2000万个转录本。
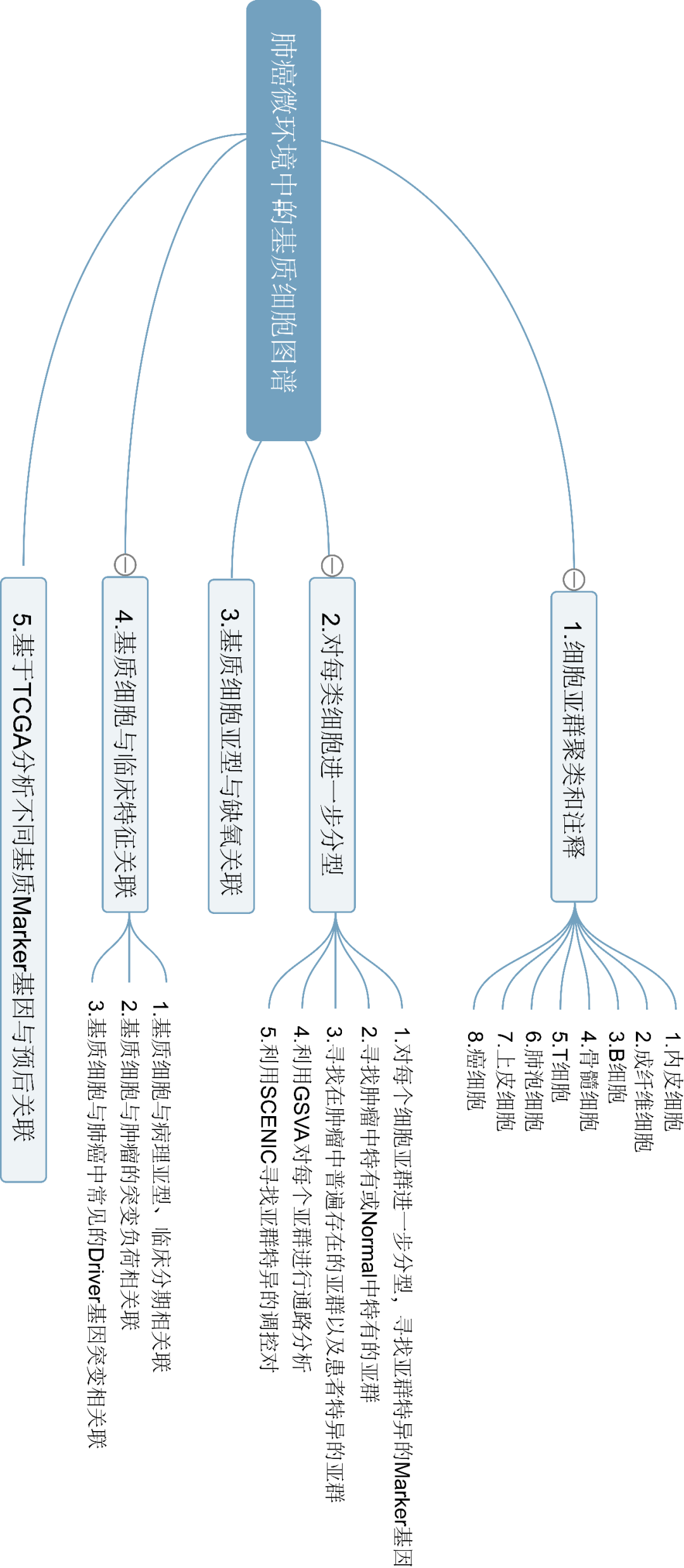
利用2192个高变基因进行主成分分析,确定了8个不同的亚群:内皮细胞、成纤维细胞、B细胞、骨髓细胞、T细胞、肺泡细胞、上皮细胞、癌细胞。
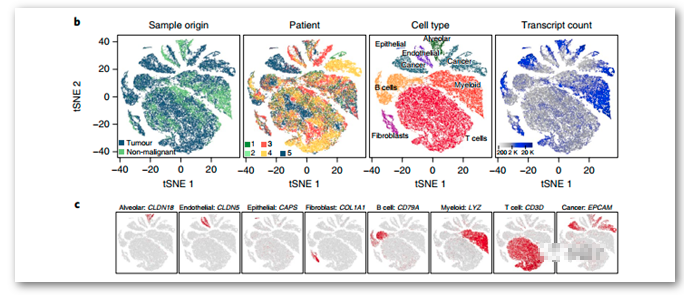
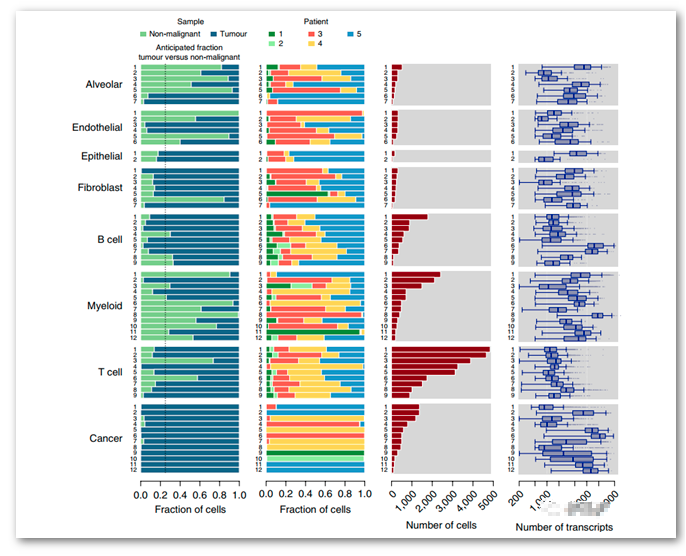
进一步对每个亚群再次聚类,划分为52种不同的基质细胞亚群和12种癌细胞亚群。
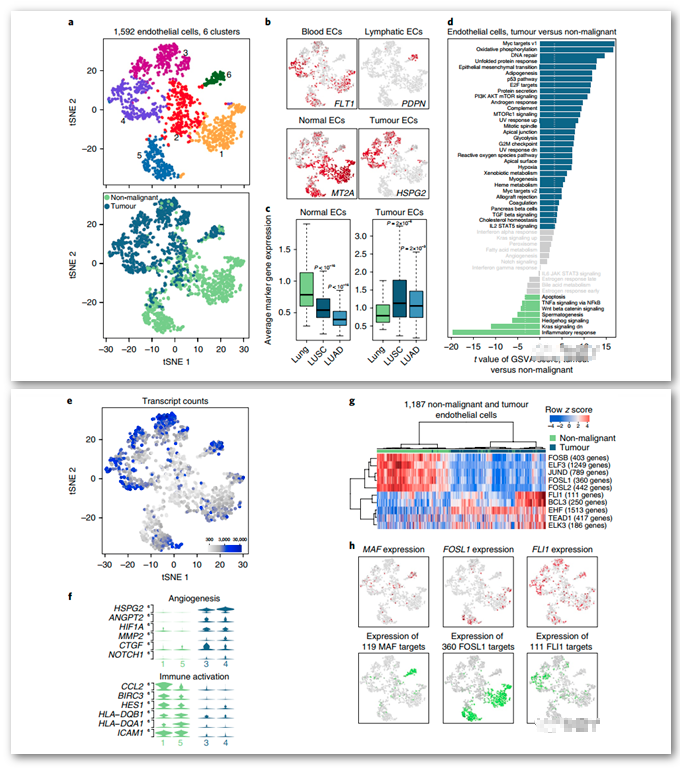
内皮细胞进一步划分为6个亚型:
淋巴管内皮细胞 (PDPN 和 PROX1)
血管内皮细胞 (FLT1+)
2个来源于肿瘤的内皮细胞 (IGFBP3+ 和 SPRY1+)
2个来源于非肿瘤的内皮细胞 (MT2A+ 和 EDNRB+)
肿瘤来源的内皮细胞转录本表达丰度高于正常组织来源的转录本。
通路分析发现肿瘤来源的内皮细胞的代谢通路上调,而免疫活性的通路下调。其中下调的基因包括抗原呈递基因 (CCL2)、趋化基因 (ICAM1)以及免疫归巢基因(HLA-DQA1, HLA-DQB1)。该结果说明肿瘤内皮细胞受到免疫微环境的影响,下调抗原呈递和免疫细胞归巢活性,进而有利于肿瘤的免疫耐受。
在肿瘤的淋巴内皮细胞中,利用SCENIC的方法,发现了可能导致肿瘤特异性表型以及削弱免疫活性的基因调控对。
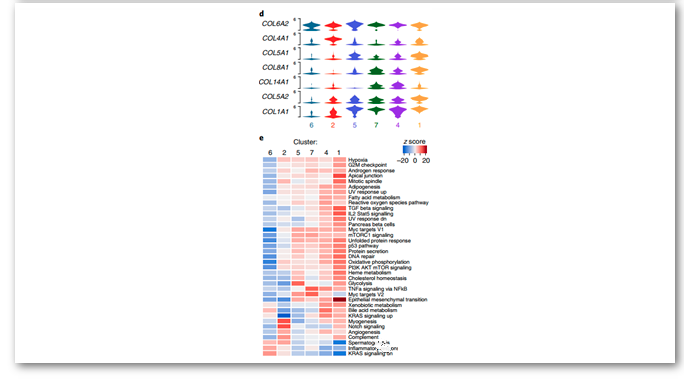
成纤维细胞可进一步划分为6个亚型:
肿瘤来源的细胞特异性表达了胶原蛋白和细胞外基质的分子(COL10A1,COL4A1)
而正常组织来源的成纤维细胞中有更高的弹性蛋白表达、较低的胶原蛋白表达
通路分析发现其中一个亚型具有上皮-间质转换(EMT)的特征,伴随着细胞外基质蛋白marker的高表达以及TGF-β基因的表达。
利用SCENIC寻找每个成纤维细胞亚型特异的基因调控对,FOXO1和MSC调控的基因在Cluster1中下调,而MEF2C和ELK3调控的基因在Cluster2中上调,说明不同来源的成纤维转录因子调控对的获悉不同,进而导致不同亚型的成纤维细胞有其特异的功能。

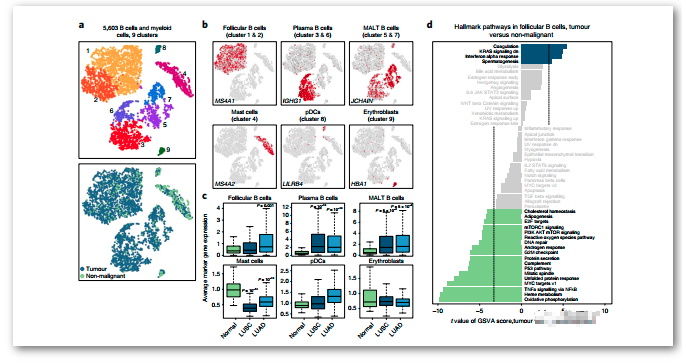
B 细胞可进一步划分为9个亚型:
滤泡型B细胞 (MS4A1, CXCR4, HLA-DRs)
浆细胞(immunoglobulin gamma)
MALT边缘区B细胞 (immunoglobulins A,M, JCHAIN)
大部分的B细胞都来源于肿瘤。
在滤泡型B细胞亚群中,负责氧化磷酸化、细胞增殖以及生物产能的基因marker在肿瘤中表达减弱,而肿瘤相关的滤泡型B细胞转录本表达普遍更低,说明在肿瘤中滤泡B细胞出现了耗竭。
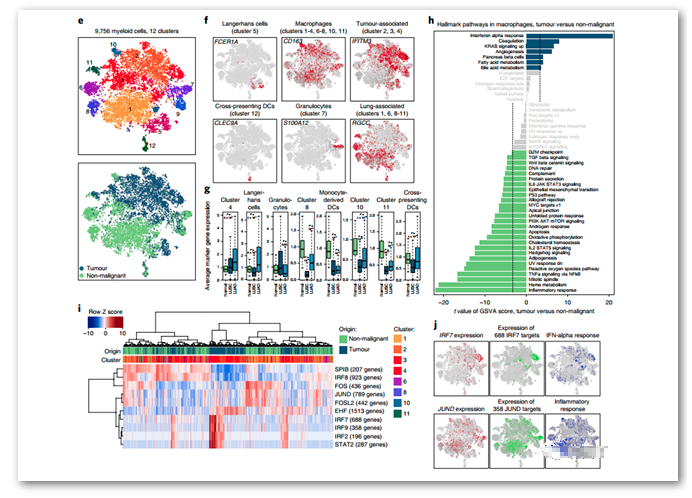
髓系细胞可进一步划分为12个亚群:
粒细胞 (S100A12+)
朗格汉斯细胞 (CD207+)
单核来源的树突状细胞 (FCGR3A+,CYTIP+)
交叉呈递的树突状细胞 (CLEC9A+,XCR1+)
CD163+和CD68+的巨噬细胞
大多数亚群的细胞都来源于非肿瘤组织。
朗格汉斯细胞簇在肿瘤和非肿瘤中数目类似。
通路分析在发现来源于肿瘤的巨噬细胞簇中炎症反应减弱、TNF-a诱导的细胞增殖能力不足,活性氧产生的通路下调,呈现出M2-like的巨噬细胞特征。
利用SCENIC,在肿瘤中发现了负责M2样巨噬细胞极化的基因调控对。
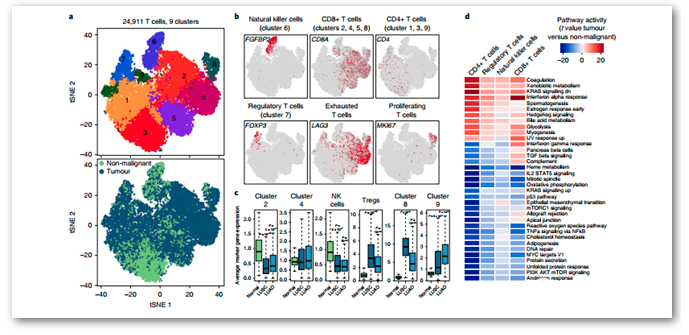
T细胞可进一步划分为9个亚群:
Treg细胞 (FOXP3+)
NK细胞及NKT细胞 (FGFBP2)
CD8+T细胞 (CD8A+)
CD4+T细胞 (CD4+)
通路分析发现肿瘤来源的T细胞和正常组织来源的T细胞类似,都表现出糖酵解功能增加和氧化磷酸化功能减弱。
CD8+T细胞的亚群中,表现出较强的增殖能力、移植排斥的反应,Myc活性等,且免疫检查点抑制剂的表达也较高。
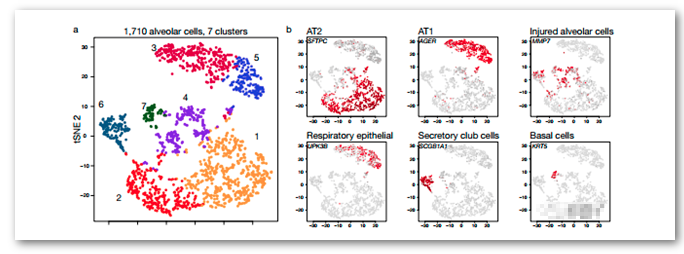
肺泡细胞可进一步划分9个亚群:
I型肺泡上皮细胞 (AGER, CAV1)
II型肺泡上皮细胞 (SFTPC, ABCA3)
棒状细胞 (SCGB1A1)
基底细胞 (KRT15)
其中I型肺泡上皮细胞、II型肺泡上皮细胞,以及呼吸道表皮细胞只肿瘤中出现。
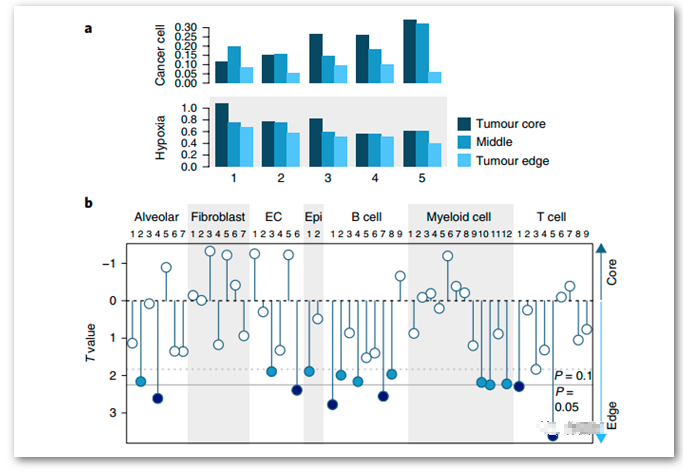
缺氧与是肿瘤行为的表现,包括血管生成、转移、代谢重编程以及免疫逃逸。
研究人员进一步按照肿瘤的部位将样本分为:肿瘤核心区域、肿瘤边缘区域、以及中间区域。发现肿瘤核心区域有更多的癌细胞。
关注不同部位的缺氧情况,发现肿瘤核心区域表现出最强的缺氧现象,其次是中间部位、边缘部位。
将不同部位的肿瘤细胞与每种类型细胞数目做线性拟合,发现大多数的基质细胞亚型富集在肿瘤边缘,并且处于常氧的环境中。
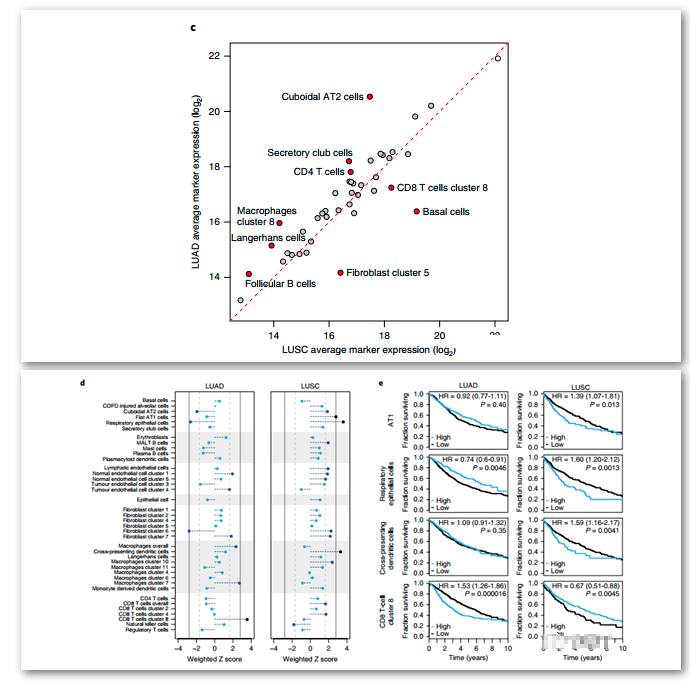
9. 基质细胞亚型关联临床信息
分析LUAD和LUSC中特异性的基质细胞亚型,发现LUAD来源于AT2的细胞而LUSC来源于基底细胞。
观察不同分析下,LUSC和LUAD的基质亚群特征,发现晚期的LUSC间质成分减少,而LUAD在不同分期下未发现明显规律。
通过TCGA数据库以及其它外部的RNASeq数据,发现在LUSC中基质marker基因的表达可以反映LUSC的预后状态。
I型肺泡上皮细胞、呼吸道上皮细胞以及交叉树突状细胞的marker基因高表达预示着LUSC患者生存较差。而CD8+T细胞marker基因高表达反映了LUAD患者的生存较差。
小编总结