CHM:婴儿出生后第一年肠道微生物组的动态变化和稳定
Dynamics and Stabilization of the Human Gut Microbiome during the First Year of Life
原文链接:https://www.cell.com/cell-host-microbe/fulltext/S1931-3128(15)00162-6
Cell Host and Microbe [IF:15.927]
DOI: 10.1016/j.chom.2015.04.004
Resource 2015-05-13
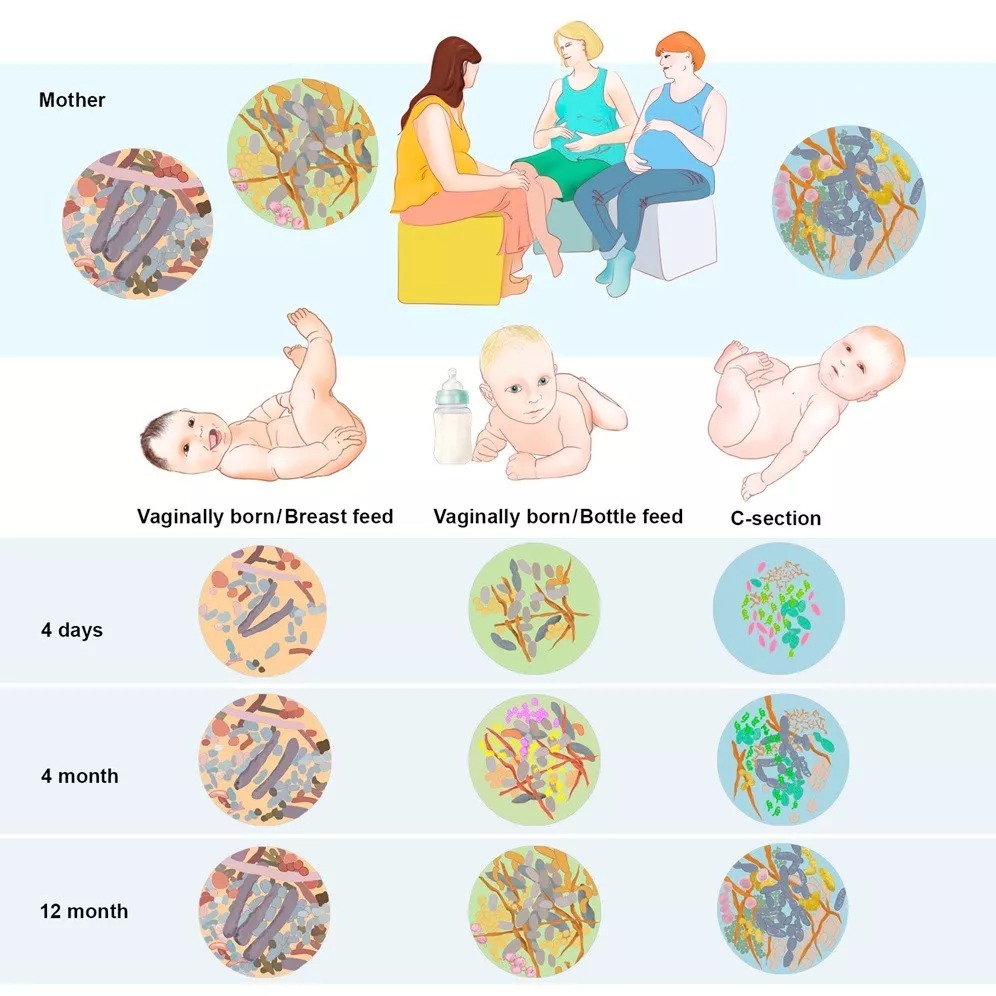
图形摘要:Bäckhed等人评估了98名瑞典母亲及其婴儿在出生第一年的肠道菌群。停止母乳喂养是决定肠道微生物群成熟的主要因素,特征物种的明显变化是其功能成熟的标志。
热心肠日报
链接:https://www.mr-gut.cn/papers/read/1037093792
Cell子刊:出生第一年,人的肠道菌群会怎么变?(资源)
原标题:人类出生后第一年肠道微生物的动态变化与稳定过程
华大基因参与的重磅研究:
①测定了98个妈妈和她们孩子出生后第一年的肠道微生物;
②断奶促使婴儿肠道微生物成熟;
③特征种的转变证明婴儿肠道微生物的转化是非随机的;
④营养的转变和异生物质代谢表明肠道微生物成熟;
⑤剖腹产婴儿的肠道微生物与妈妈最不相似。
研究总结
肠道微生态对人类健康具有重要的作用,但是还没有定量地或者从功能的角度研究生命早期的肠道微生态的建立过程。我们应用宏基因组分析大规模瑞典婴儿和他们母亲的粪便样品,描述这些婴儿在出生后第一年内的肠道微生物组,评估出生模式和喂养方式的影响。与经过阴道分娩的婴儿不同,剖腹产的婴儿肠道微生物组表现出与母亲的肠道微生物组显著更低的相似性。营养对于早期的肠道微生态的组成和功能也有重要的作用。停止母乳喂养对于形成一个更像成年人成熟的肠道微生态是必需的。在不同时期,肠道组成和生态网络都有不同的特点,与功能的成熟过程相一致。我们的发现建立了一个在生命早期肠道微生物组和人类身体相互作用的框架。
研究背景
对于人类健康,人体肠道微生态是一个很重要的环境因素,在代谢、免疫、发育和宿主行为方面都发挥了进化上保守的作用。虽然很多研究都关注于建立成年人肠道微生物组的参考基因集以及建立与复杂疾病的关系,但是婴儿肠道微生物组的研究却仅限于基于培养的计数、基于16S的分析和小样本量的研究。因此,还没有让人满意的在生命早期塑造肠道微生态的关键因素的研究。
从生态学的角度看,婴儿肠道的定殖代表了受到饮食和医疗因素影响的微生物群落的重新组合。但是,尚不清楚这些因素如何影响婴儿肠道菌群整体的组成和功能,也不清楚随着肠道环境的变化,不同的微生物如何相互合作或者竞争。
在这篇文章中,我们对98名足月的瑞典婴儿和他们的母亲进行宏基因组鸟枪测序,组装肠道微生物基因组,并展示出生后第一年中各个时间段的标志性特点和功能特征。另外,我们还制作了一份正在发展的微生物组的参考基因集,这可能是重要的研究工具。
研究结果
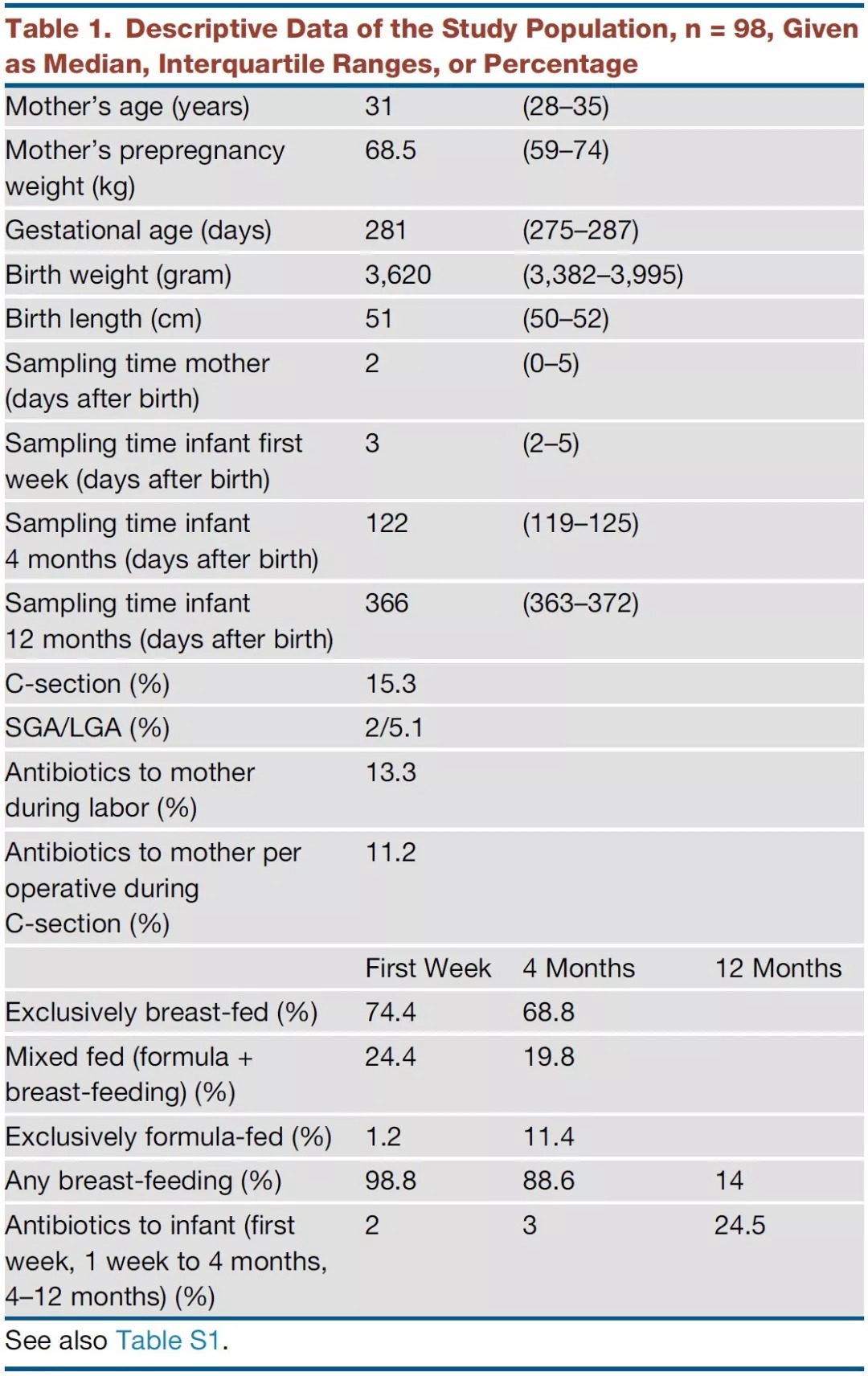
表1. 研究人群的描述
样本量 n=98,给出中位数、四分位数之间的范围或百分比
组装婴儿肠道微生物组的基因组
Genomes Assembled from the Infants’ Gut Microbiome
为了表征婴儿肠道微生物态,我们对98名正常妊娠后分娩的母亲和他们的婴儿(其中15名剖腹产) 在出生后的第一天、4个月大和12个月大的时的粪便样本进行了鸟枪法测序。所有婴儿出生时的胎龄为37 - 42周,大多数父母来自瑞典( 12 / 98的婴儿至少有一名父母来自非瑞典)。总的来说,我们生成了1.52 Tb高质量的双端读取的reads数据(平均每个样本3.99 Gb )。基于从头组装(de novo assembly)和宏基因组的基因预测,为每个时间点构建基因图谱,并使用KEGG (Kyoto Encyclopedia of Genes and Genomes)数据库进行功能注释。
为了从结构上组织和在分类上注释婴儿样本中的基因,我们设计了一种策略,在他们的肠道宏基因组中重建大多数细菌或古基因组。我们根据样本间的丰度差异,采用分箱(binning)组装好的重叠群(contigs),重新(de novo)组装了4356个基因组。来自NCBI细菌/古细菌基因组数据库的1147个基因组补充了这些新组装的基因组。所有基因组随后聚类成690个独特的宏基因组操作分类单元(MetaOTUs ),相当于物种级别。Firmicutes 和 Bacteroidetes 是最普遍的门,其次是Actinobacteria和Proteobacteria。总共有373个MetaOTUs被标注为物种,其余317个代表了与已知物种相关的新物种。尽管不如NCBI的基因组完整,但新的MetaOTUs显示出对保守单拷贝基因的良好覆盖。从婴儿样本中构建的大多数MetaOTUs也在母亲身上发现,在母亲的样品中经常显示出更高的丰度。
主坐标轴分析(PCoA,基于 unweighted UniFrac 距离)显示,样本按年龄分组,并显示12个月大的婴儿与母亲最相似。我们观察到随着时间的推移,α-多样性增加,但β-多样性减少,表明这是一个更加复杂和更不异质的群落。在年龄较大的婴儿中识别出增加的微生物基因组数量也支持了复杂性上升的这一结论。
图1. 剖腹产婴儿与母亲肠道菌群的相似性降低
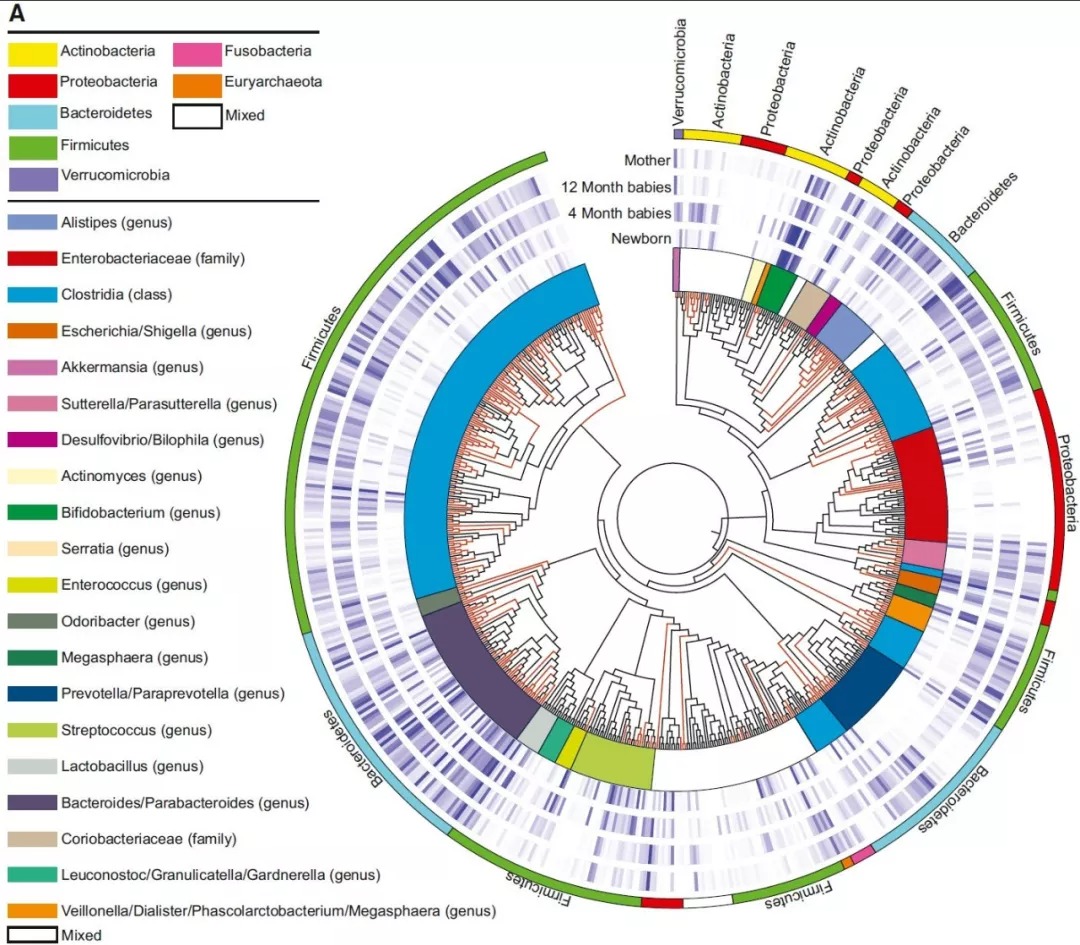
(A)由至少一个样本中存在的625个MetaOTUs构建的系统发育树(在所构建的690个MetaOTUs中,65个显示零丰度,即MetaOTUs中的所有基因组在所有样本中都平均相对丰度 < 0.005)。根据邻域连接方法,利用MetaOTU对的平均基因组MUMi距离构建该树。新的MetaOTUs展示为红色的树枝。最外圆的色块表示门,内圆的色块表示除肠杆菌科、梭状芽孢杆菌科和分支杆菌科(科)外的属。热图圈显示新生儿、4个月大的婴儿、12个月大的婴儿和母亲的每一个MetaOTUs的相对丰度。
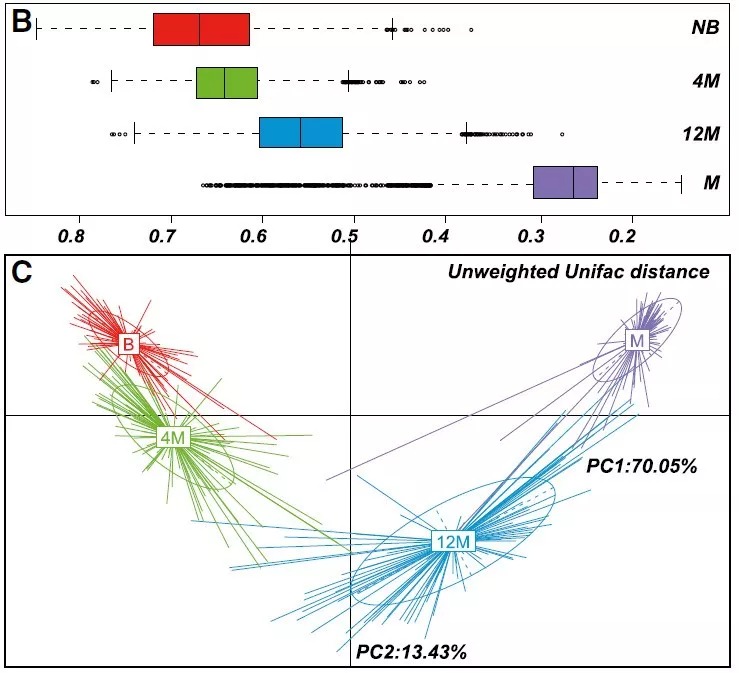
(b)婴儿和母亲MetaOTU组成(NB,新生儿;4M,4个月大的婴儿;12M,12个月大的婴儿;M,母亲)之间未加权unifrac距离的箱线图。
(c)PCoA的散点图,基于每个样本中mMetaOTU的未加权unifrac距离。
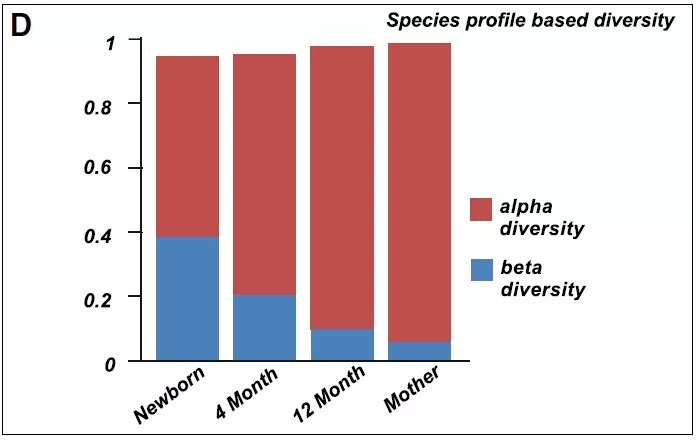
(d)a-多样性和b-多样性是由rao的多样性分解决定的,考虑到系统发育和相对丰度。另见图S1和表S2。
母亲肠道微生物的遗传
Inheritance of the Mother’s Gut Microbiome
出生模式对新生儿的微生物的物种组成有很大的影响。与从阴道出生的婴儿相比,剖腹产的新生儿粪便微生物群富含Enterobacter hormaechei/E. cancerogenus, Haemophilus parainfluenzae/H.aegyptius/H. influenzae/H. haemolyticus, Staphylococcus saprophyticus/S. lugdunensis/S. aureus, Streptococcus australis 和 Veillonella dispar/V的MetaOTUs,这表明皮肤、口腔微生物以及出生过程中周围环境中的细菌是第一批在这些婴儿中定殖的细菌。相比之下,阴道分娩的新生儿肠道微生物富含Bacteroides、Bifidobacterium、Parabacteroides和Escherichia/Shigella的微生物,它们也是新生儿肠道微生物中最丰富的成员。然而,Escherichia/Shigella是新生儿中最丰富的属,富含这些菌的新生儿的取样时间早于以Bacteroides或Bifidobacterium为主的新生儿的取样时间,这与胎粪和胎盘中大肠杆菌DNA的高浓度相一致。因此,剖腹产的新生儿中Escherichia/Shigella的低丰度可能反映出,与阴道出生的新生儿相比采样稍晚(出生后4.9±1.9天与3.6±2.8天)。出生方式之间的差异在4个月和12个月大时逐渐减小,但是与阴道分娩的婴儿相比,剖腹产婴儿的差异仍然更大。与阴道分娩的婴儿相比, Bacteroides,特别是B. ovatus/B. xylanisolvens, B. thetaiotaomicron, B. uniformis, and B. vulgatus/B. dorei,在剖腹产新生儿中不太普遍或缺失,这种差异在4个月和12个月大时依然存在。
为了调查母亲的肠道微生态在多大程度上促进了婴儿肠道微生态的建立,我们比较了新生儿和母亲的肠道细菌。在阴道分娩的新生儿存在的187个分类注释的MetaOTUs中,有135个也在他们母亲的样品中发现了,包括重要的种,比如:Escherichia/Shigella, Bifidobacterium longum, Enterococcus faecalis, Bacteroides fragilis, B. thetaiotaomicron和Bilophila wadsworthia,这表明了垂直的母婴传播。其余的52个MetaOTUs在母亲的样品中没有找到,这些MetaOTUs在新生儿中的普及率(prevalence)较低(在不到5名新生儿中发现了42个MetaOTUs),并且通常在4个月大的婴儿中没有找到。有几个MetaOTUs在超过10个新生儿中存在,但是在他们的母亲的样品中没有发现,包括Propionibacterium acnes、Streptococcus agalactiae和Veillonella_oral_taxon_780,可能来源于其他身体部位或环境。然而,这些物种的普及率(prevalence)随着年龄的增长而下降,并在12个月时完全消失,这可能反映了他们降低的在人类肠道中持续存在的适应能力。
剖腹产新生儿肠道菌群的母婴传播会受到影响。我们发现72 % ( 135 / 187 )的阴道分娩新生儿的早期定殖细菌在自己母亲的粪便样品中发现了,而剖腹产新生儿只有41 % ( 55 / 135 )。
我们观察到一些细菌被更低频率地共享了,比如Bacteroides,但是比如Enterococcus faecalis的共享却被保留了下来。在剖腹产婴儿中也观察到Bifidobacterium在母婴中传播,但是与阴道分娩的婴儿相比,其传播频率较低,这与以前的研究一致。我们的结果表明,新生儿肠道的早期定殖细菌大多来自母亲,出生模式是足月婴儿形成早期肠道微生物态的重要因素。
图2.剖腹产婴儿与母亲肠道菌群的相似性降低
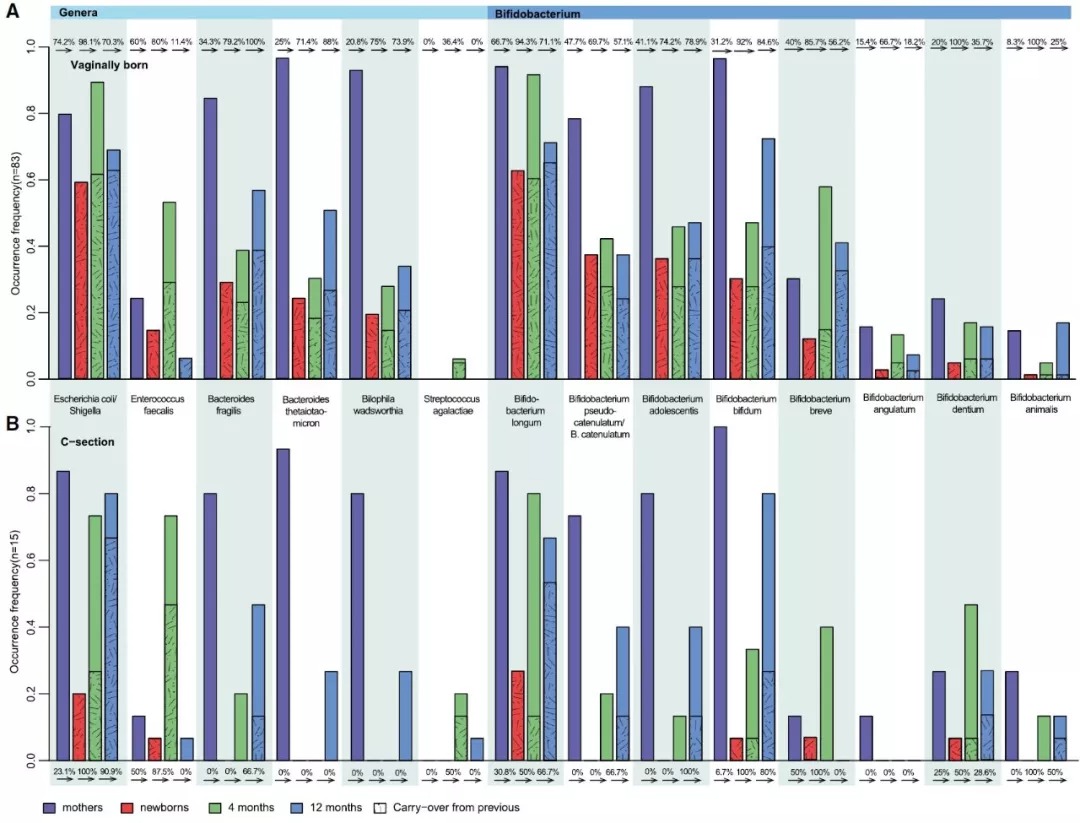
在不同阶段,被选择的MetaOTUs在阴道分娩的婴儿(A)和剖腹产婴儿(B)出现频率。在每个栏中,阴影线标记了与前一阶段共享的部分,即新生儿与母亲共享,4个月大的样本与相应新生儿样本共享,12个月大的样本与相应4个月大的样本共享。这种可能结转(carryovers)的百分比如箭头所示。另见图S2和表S3。
肠道微生物功能的成熟
Functional Maturation of the Gut Microbiome
为了确定婴儿出生后第一年肠道微生物的功能是如何发展的,我们使用KEGG 同源注释阴道分娩的婴儿的肠道微生物。在出生后的第一年,新生儿相对简单的肠道微生物进化成更复杂和更像成人的结构,这与以前的研究是一致的。我们观察到1岁孩子与母亲肠道宏基因组的功能相似性增加,个体间差异减少。
人类肠道微生物是抗生素抗性基因的储存库,被称为抗性组。在这里,我们观察到新生儿的微生物中已经存在抗生素的抗性基因,这可能是Proteobacteria的DNA相对富集的结果,其基因组包含高水平的抗生素抗性基因。新生儿微生物中超过90 %的基因与对杆菌肽(bacitracin)、四环素(tetracycline)和大环内酯类(macrolides)的耐药性有关,这些耐药性在成人肠道中也非常普遍。对卡那霉素(kanamycin)等抗生素的耐药性随着年龄的增长而增加,在母亲的微生物组中出现率(occurrence)最高。五名婴儿在分娩后4个月内接受了抗生素治疗,这导致了在4个月时微生物组成的轻微变化,但并没有影响12个月内微生物群中的抗生素抗性基因库。然而,与阴道分娩的婴儿相比,剖腹产婴儿的微生物往往含有更大比例的抗生素抗性基因。
宏基因组分析还揭示了在取样时,婴儿肠道微生物对不同能源的利用情况。特别是,新生儿微生物中碳水化合物摄取的磷酸转移酶系统(phosphotransferase system,PTS )基因丰富,而乳糖特异性转运蛋白(lactose-specific transporter)在4个月大的婴儿中最为丰富,这与以牛奶为主的饮食相一致。新生儿和4个月大的婴儿的微生物富含降解母乳中糖分所需的基因,母乳是这两组婴儿的主要营养来源。相比之下,β-葡萄糖苷特异性转运蛋白(β-glucoside-specific transporters)在4个月大和12个月大的婴儿中最为丰富。相应地,12个月大婴儿的微生物富含与复合糖和淀粉降解有关的基因,并与B. thetaiotaomicron的丰度增加有关,目前已知这种菌含有种类繁多的多聚糖降解酶(glycan-degrading enzymes)和与碳水化合物代谢相关的模块(module)。B. thetaiotaomicron和参与果胶降解的主要的酶-果胶酯酶(pectinesterase),在12个月大的婴儿中含量最高,这可能是由于在这个年龄摄入了更多富含果胶的固体或半固体食物。
由于成熟婴儿肠道中细菌代谢功能的连续性,我们观察到Desulfovibrio spp和Methanobrevibacter smithii在母亲样品中大量存在,但在婴儿中缺乏,只有两个12个月大的婴儿被Methanobrevibacter smithii定殖。这一发现与母亲内微生物组甲烷产生能力的增加相一致,这与成人微生物组发酵能力的增强相关,成人微生物需要将氢气转化为甲烷或其他副产品。
随着婴儿年龄的增长,微生物群暴露于更多种类的食物中,这与碳代谢中基因的丰富有关。例如,相比新生儿,4个月大和12个月大的婴儿更富含丙酮酸代谢的KO模块,丙酮酸:铁氧还蛋白氧化还原酶催化丙酮酸(pyruvate: ferredoxin oxidoreductase)转化为乙酰辅酶A(acetyl-CoA)。相比之下,新生儿相对氧化的肠道环境使肠道微生物能够利用TCA循环产生能量和新陈代谢,与4个月大和12个月大的婴儿和母亲相比,新生儿TCA循环KO模块的丰富程度也表明了这一点。总的来说,我们的结果表明,随着婴儿年龄的增长,微生物适应了可获得的能量来源。
肠道微生物群是维生素的重要生产者。瑞典所有新生儿都接受预防性维生素K注射,以避免典型的出血性疾病。我们观察到新生儿维生素K2 (menaquinone)合成基因含量丰富,这与已知维生素K2生产者——Bacteroides和Escherichia/Shigella的高丰度相关。维生素K2对骨骼和心脏健康非常重要,最近发现微生物群可以调节骨骼的稳态。维生素A(retinol)的代谢在新生儿中也最为丰富,这暗示了在视觉、骨骼和牙齿等几个基本发育过程中发挥了作用。身体需要的所谓的B族维生素将营养物质转化为葡萄糖并产生能量。叶酸(Folate,维生素B9 )是DNA合成和修复所必需的B族维生素之一。新生儿显著富含叶酸合成的基因。新生儿中吡哆醛(pyridoxal,维生素B6 )和生物素(biotin,维生素B7 )合成基因也显著丰富。相比之下,硫胺素(thiamine)、泛酸(pantothenate)和钴胺素(cobalamin)(分别是维生素B1、B5和B12 )合成基因随着年龄的增长而增加,这与之前的研究一致。然而,新生儿宏基因组中维生素B12转运系统的模块显著增加,但随年龄增长而减少。同样,铁、氯高铁血红素(hemin)和亚铁血红素(heme)的转运体也在新生儿的微生物组中增加,这些转运体与维生素B12的合成有关,对铁代谢很重要。
KOs在氨基酸代谢中的表现也随年龄变化。新生儿的微生物组中所有必需氨基酸的转运系统都很高,并且在4个月大之前,水平一直很高。按每公斤体重计算的蛋白质需求随着年龄的增长逐渐减少,直到断奶,这可能会同时影响对氨基酸运输系统的需求,与我们的数据一致。蛋氨酸(methionine)降解、赖氨酸(lysine)生物合成、亮氨酸(leucine)和色氨酸(tryptophan)的通路或模块随着时间的推移而增加,并在12个月大时达到与母亲相当的水平。最后,氨基酸神经递质GABA (gamma-aminobutyrate,γ-氨基丁酸)和褪黑激素(hormone melatonin)合成和代谢基因在新生儿、4个月大和12个月大的婴儿中显示出不同程度的富集。在人类中,褪黑激素在昼夜节律系统中起作用。新生儿没有建立起的褪黑激素昼夜节律,这种节律在3 - 4个月大时出现,并在儿童时期成熟,这与我们对褪黑激素生物合成波动的观察一致。
图3. 阴道分娩的婴儿在出生第一年的肠道微生物的功能成熟

(A) 与母亲(M)相比,新生儿(NB)、4个月大婴儿(4M)或12个月大婴儿(12M)的基因组中富含KO途径的热图和分层聚类。绘制了至少在一个队列中报道得分大于1.6的KO途径。
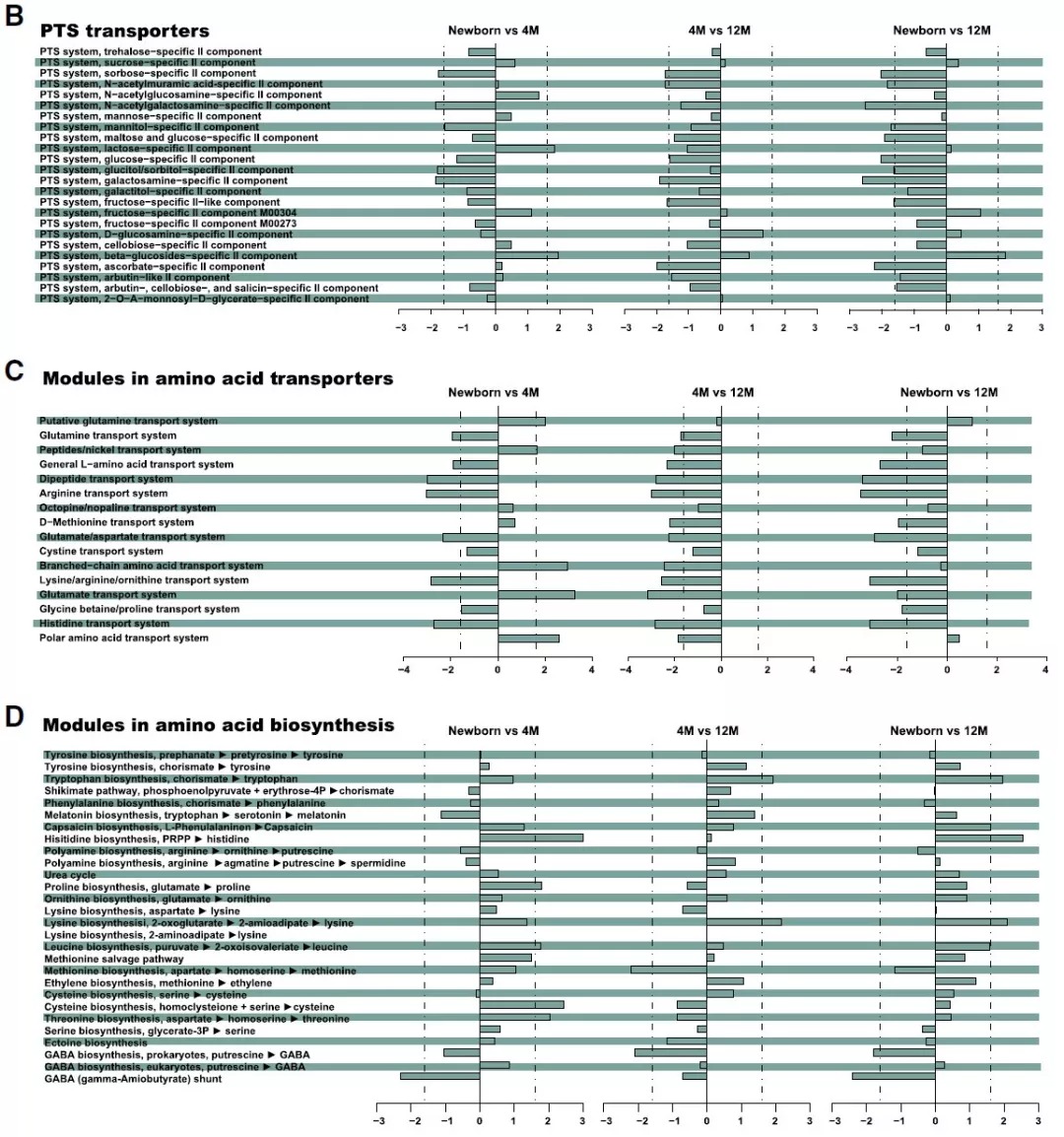
(B–D) 比较阴道分娩的婴儿中磷酸转移酶系统(PTS)转运体模块(B)、氨基酸转运体(C)或氨基酸生物合成模块(D)的丰度的报告评分条形图,(新生儿n = 81,4个月大婴儿、12个月大婴儿和母亲n = 83)。仅显示在宏基因组中发现的KOs超过40%的模块。虚线表示报告分数为1.6,这是在此类分析中使用的显著差异的阈值(详见补充实验方法)。另见图S3和图4以及表S4。
每个阶段的特征类群
Signature Taxa at Each Stage
接下来,我们描述了肠道微生物群在出生第一年的独特特征,并使用一种既定的生态学方法,既考虑不同分类群的丰富度,又考虑了普及率(prevalence),定义了阴道分娩和剖腹产婴儿的特征分类群。在阴道分娩组中,新生儿携带来自Enterococcus、Escherichia/Shigella、Streptococcus和Rothia的细菌,表明肠道环境相对有氧。Bifidobacterium、Lactobacillus、Collinsella、Granulicatella和Veillonella属被鉴定为4个月大的微生物群的特征类群,这表明在主要由母乳组成的饮食中,氧浓度降低,乳酸的产生和利用增加。12个月时的特征属包括新生儿中发现的细菌,即Bacteroides和在4个月时出现的细菌,例如Anaerostipes、Anaerotruncus和Clostridiales,以及仅在12个月时出现的细菌,即Eikenella。这些微生物许多都能有效降解膳食纤维,产生短链脂肪酸。这表明随着碳水化合物降解能力的增强,肠道环境更像成年人。剖腹产的婴儿似乎在每个阶段都不同于阴道分娩的婴儿,例如,Blautia和Prevotella是12个月时的特征类群,但是没有在其母亲体内发现。
此外,我们还观察到,随着阴道分娩婴儿肠道微生物群进入更成熟的阶段,生态网络会被重塑。注释为Escherichia 和 Staphylococcus的MetaOTUs的相对丰度呈负相关,但在4个月内呈正相关。许多兼性厌氧菌与新生儿中的许多专性厌氧菌呈正相关,但在4个月时,它们的相关性大大降低或呈负相关,这可能反映了氧浓度的降低和更明确的生态位。在四个月大时,Veillonella atypica、Peptoniphilus和Anaerococcus之间从正相关到负相关的转变也可能表明Peptoniphilus和Anaerococcus的丁酸盐产量增加,而不是乳酸盐产量增加。Bifidobacterium longum,一种4个月时的标志性的MetaOTU ,显示了与B. adolescentis的正相关到负相关的转变,表明竞争或多样化的选择。从4个月到12个月, Ruminococcus gnavus有数量最多的显著变化的连接。在12个月大的婴儿中,R. gnavus和Roseburia inulinivorans都是典型的MetaOTUs。R. gnavus可以利用宿主的粘蛋白多糖,并且已经发现在患有克罗恩病的成年患者体内会增加,而Roseburia inulinivorans生长在益生元膳食纤维菊粉上。总的来说,这些结果都表明,随着婴儿的长大,环境因素和饮食的变化,肠道微生物态的组成和网络结构都会随之演化。
图4. 各阶段特征属的动态
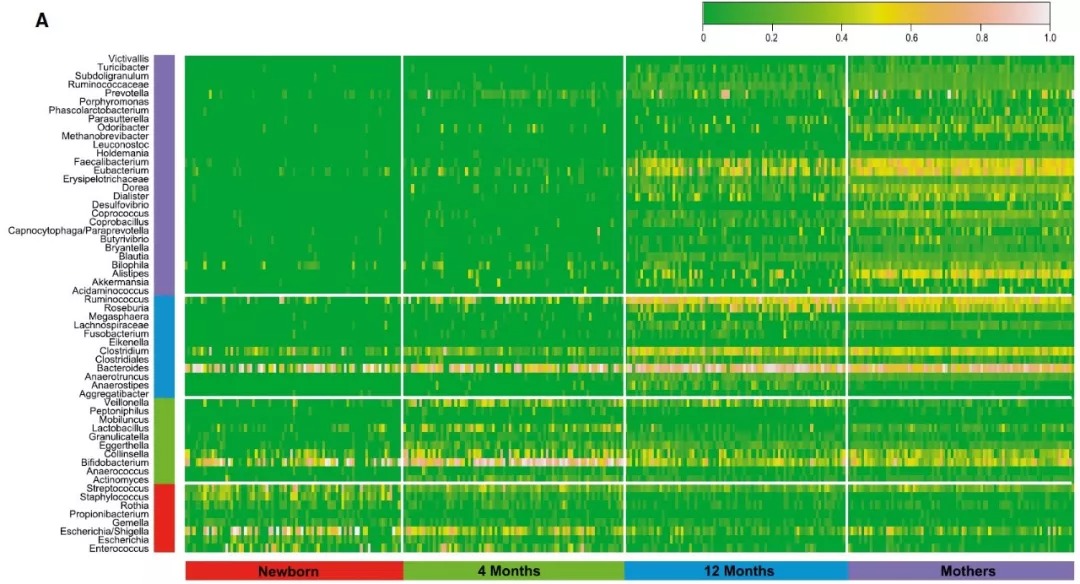
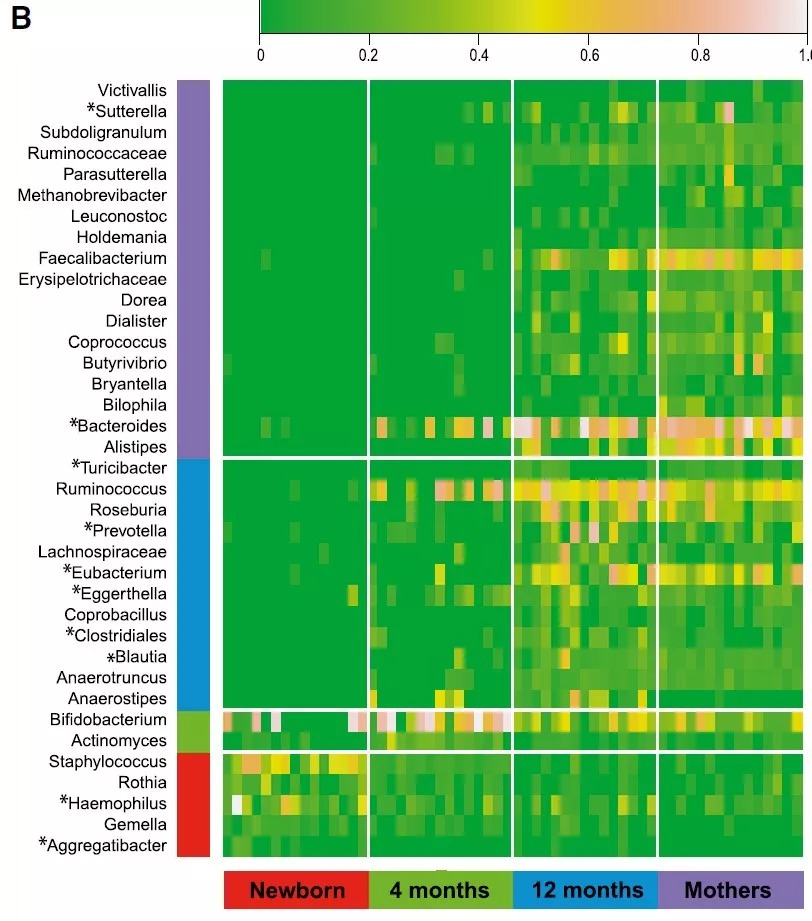
阴道分娩(A)或剖腹产(B)出生的婴儿在出生时、4个月大、12个月大及其母亲中特征属的相对丰度的热图。每个垂直通道对应一个样本。与阴道出生的婴儿相比,仅在剖腹产的婴儿上观察到的或在不同阶发生变化的特征属用星号突出显示。另见表S5。
喂养模式和肠道微生物的成熟
Feeding Pattern and Gut Microbial Maturation
为了更好地评估不同因素对婴儿出生后第一年肠道微生物群建立的影响,我们分析了母乳喂养对阴道分娩婴儿的影响。据报道,婴儿出生后第一周的喂养方式是完全母乳喂养或混合喂养,对新生儿微生物群没有显著影响。我们评估了与不同喂养方式一致的肠道微生物成熟和时间年龄的潜在差异。随机森林模型接受了完全母乳喂养的新生儿( n = 49,阴道分娩,在4至12个月断奶)所有的MetaOTUs的相对丰度的训练,64个MetaOTUs(其中27个是新物种)被选为肠道微生物年龄的标志物种。在除母乳外还接受配方奶粉的婴儿组成的测试组中,新生儿和4个月的年龄估计数通常比纯母乳喂养的新生儿更成熟。使用相同的模型,我们注意到剖腹产的婴儿出生时和4个月大的肠道微生物群也比阴道分娩的婴儿更成熟。
在4个月大的时候,我们注意到完全母乳喂养和纯配方奶喂养的婴儿的肠道微生物在MetaOTU水平存在明显差异。纯母乳喂养的婴儿益生菌的分类群水平更高,如L. johnsonii/L.gasseri、L. paracasei/L. casei, 和 B. longum。配方奶粉喂养的四个月大的婴儿有更高水平的Clostridium difficile, Granulicatella adiacens, Citrobacter spp., Enterobacter cloacae和Bilophila wadsworthia,与以前的研究一致。从新生儿到4个月大,B. adolescentis在配方奶粉喂养的婴儿中有所增加,与B. longum的相关关系从正相关变为负相关。尽管总体功能差异很小,配方奶粉喂养的婴儿富含PTS系统中某些转运蛋白的KO模块,并富含成人微生物群中发现的功能,如胆汁酸生物合成和甲烷生成。根据CAZy (碳水合物活性酶)数据库,配方奶粉喂养的婴儿表现出GH86、GH116、PL1和PL2的比例过高,它们是β-琼脂酶(β-agarase)或β-紫菜酶(β-porphyranase)和果胶酸裂解酶(pectate lyase)。相比之下,完全母乳喂养的婴儿的微生物群含有参与氧化磷酸化和B族维生素的合成更高水平的KO模块,如核黄素(riboflavin)、四氢叶酸(tetrahydrofolate)和生物素(biotin)和GH119 (α-淀粉酶 ,a-amylase)。
停止母乳喂养对12个月大的婴儿的微生物群有着深远的影响,并使肠道微生态向富集Bacteroides、Bilophila、RoseburiaClostridium和Anaerostipes的更像成年人的组成转变。相比之下,母乳喂养的12个月大婴儿的肠道微生物群仍以Bifidobacterium、Lactobacillus、Collinsella、Megasphaera和Veillonella为主,这些细菌以前曾在母乳中发现过。与此一致的是,这12个月大的婴儿的“微生物年龄”似乎比不再母乳喂养的婴儿要不成熟。因此,我们的结果强调了母乳喂养在出生后第一年肠道微生物群落的形成和演替中的作用。
图5. 重构不同阶段的MetaOTUs的网络图
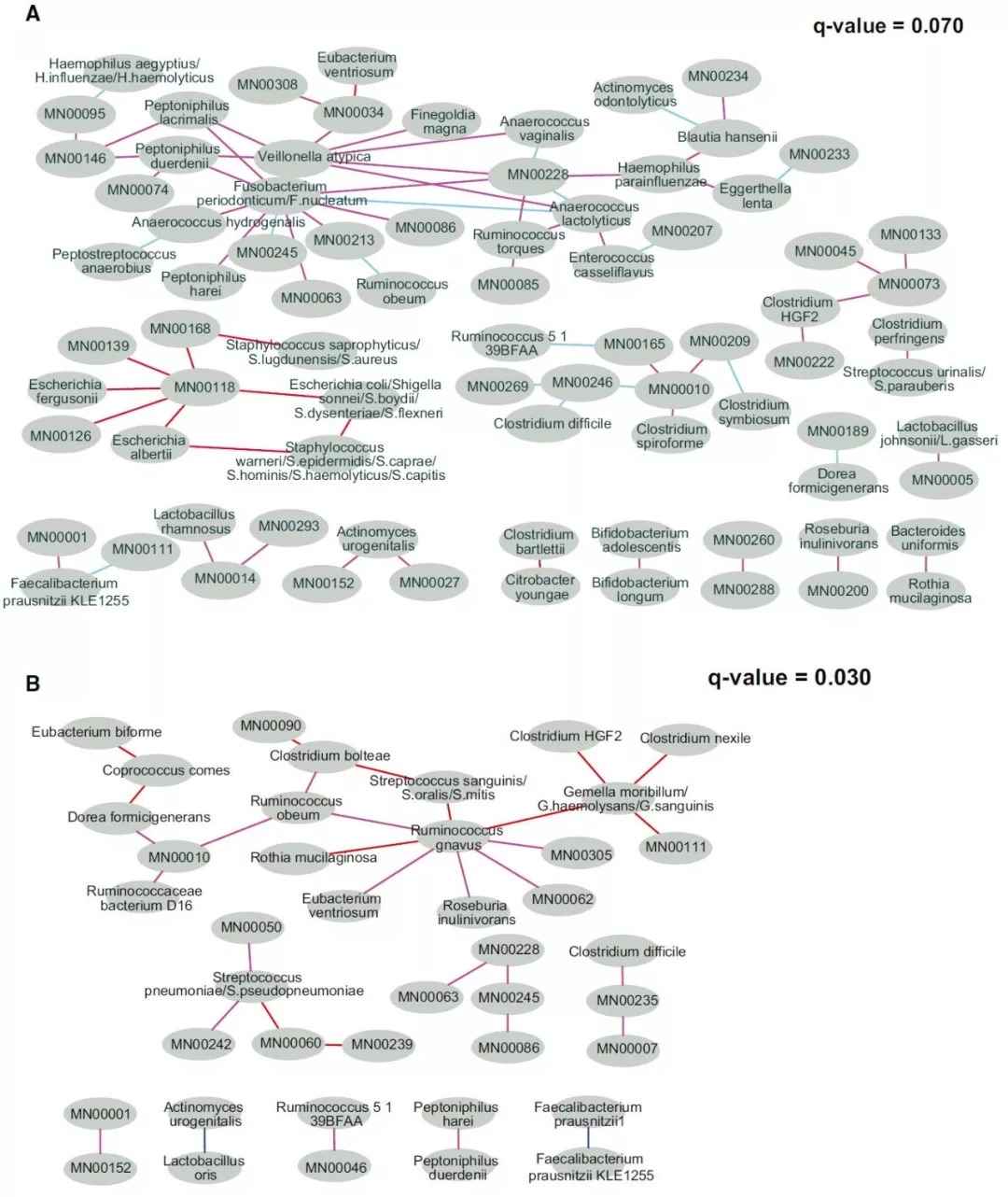
绘制了新生儿和4个月大婴儿之间(A)以及4个月和12个月大婴儿之间MetaOTUs( B )的Spearman相关性的显著差异。只考虑了阴道分娩的婴儿。比较了Spearman相关系数( cc)>0.6或<-0.6,在至少一个阶段中p<0.5,并通过置换检验(permutation test)两个阶段之间差异的显著性。对于p < 0.05,新生儿和4个月之间的q = 0.070,4到12个月之间的q = 0.030。网络的边缘(edge)是根据Spearman的cc值着色的。红色(red),cc < -0.6,然后cc > 0.6;洋红色(magenta),cc > 0.6,且 cc < -0.6;蓝色(blue),cc > 0.6,稍后更高;青色(cyan),cc > 0.6,之前更高。另见表S6。
图6. 喂养方式对微生物组的影响
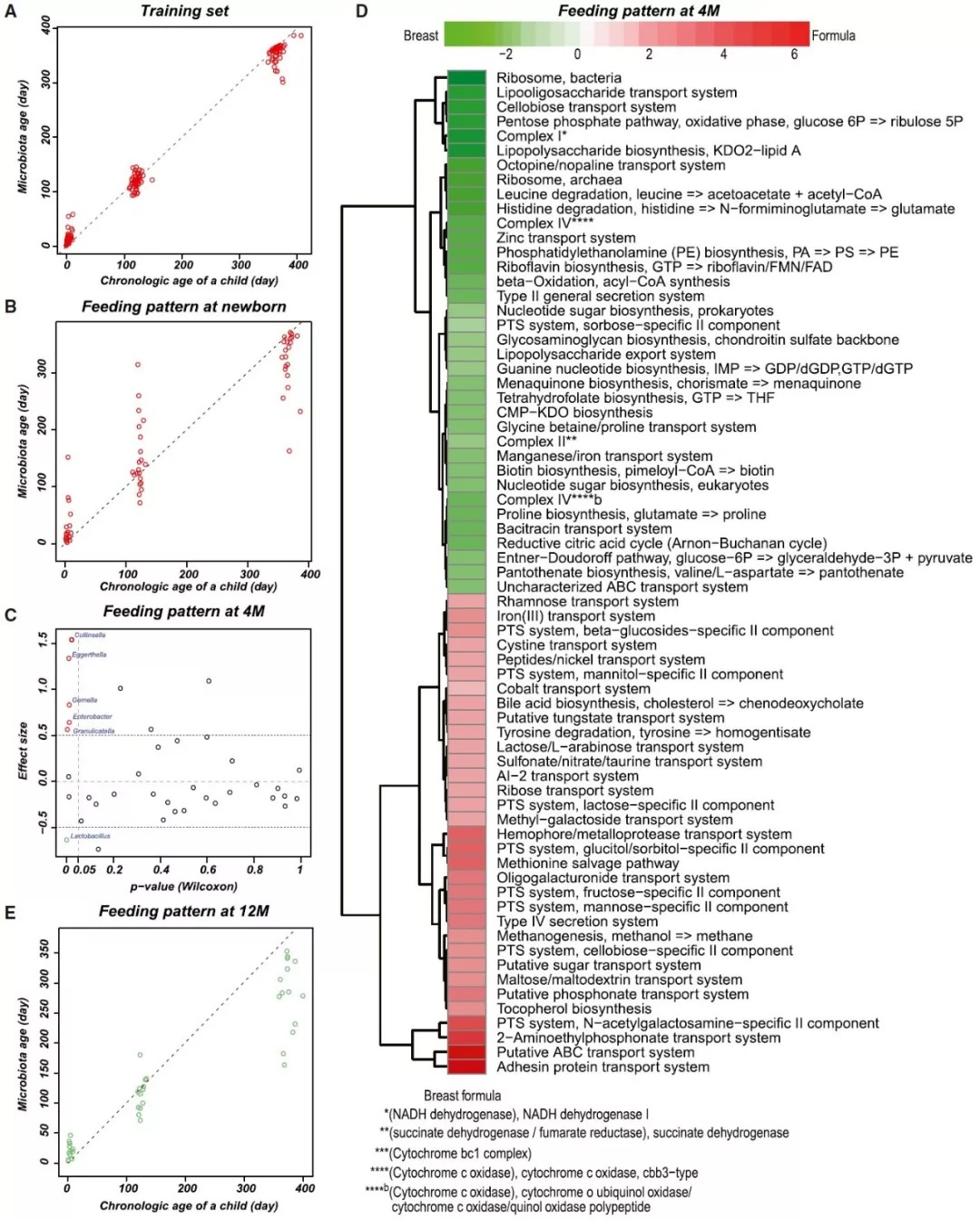
(A)训练集中微生物年龄与生理年龄关系(n=49,阴道分娩,新生儿母乳喂养,12个月停止母乳喂养)
(B)由阴道分娩的婴儿组成的试验组中微生物群年龄与时间年龄的对比(n=21);
(c)受4个月喂养模式影响的属(表S7)。正效应大小,母乳喂养(n=59);负效应大小,母乳喂养(n=8)。根据Wilcoxon秩和检验得出的p值。
(d)受4个月喂养模式影响的KO模块(报告者得分大于1.6;表S7)。绿色,富含母乳喂养(n=59);红色,富含配方奶粉喂养(n=8)。
(e)由阴道分娩的婴儿组成的试验组中,12个月时仍母乳喂养的微生物群年龄与时间年龄(新生儿为n=12;4个月和12个月为n=14)。另见图S5和表S7。
讨论
我们的研究显示了98名足月瑞典婴儿在正常足月妊娠后的第一年内肠道微生物群是如何发展的。出生模式和停止母乳喂养是推动成人肠道微生物群组装(assembly)的两个关键因素。我们观察到婴儿肠道中的非随机转变,可能是由于在群落演替期间建立厌氧环境,营养获取和微生物相互作用而诱导的。我们开发了一种MetaOTU的方法,可以鉴定超过4000种新的微生物基因组,从而使其对各种环境中微生物基因组的综合研究非常有用。
我们的结果显示,婴儿肠道微生物群的α-多样性增加,β-多样性减少,表明随着时间的推移,微生物群变得更复杂,差异也更小,与之前不同儿童和成人的横向比较所报道的结果一致。基于对16S rRNA的调查,作者得出结论,婴儿微生物群在3岁前逐渐成熟为成人肠道微生物的结构。然而,这可能更适用于马拉维和美洲印第安儿童的肠道微生物群,因为美国的1岁婴儿的肠道微生物已经像青少年一样接近成人了。在我们的瑞典队列中,12个月大的婴儿比新生儿或4个月大的新生儿更像他们的母亲。然而,1岁儿童和母亲的肠道菌群在组成和功能上仍存在差异,有待进一步成熟。
与先前对早产儿的研究一致,我们的结果表明肠道微生物组的成熟是一个非随机的过程,在每个采样年龄,可以识别出不同的特征物种以及关键微生物类群之间正、负相互作用的变化网络。然而,在早产儿中,宿主生物学(出生时的胎龄)被认为是主要的驱动因素,我们对足月婴儿的研究结果表明,分娩方式和喂养方式对肠道微生物群的组装(assembly)有重大影响。我们观察到,大多数早期定殖细菌来自母亲,在剖腹产婴儿中,重要的肠道微生物,如Bacteroides 和 Bifidobacterium,母婴垂直传播的频率较低,而皮肤和口腔中细菌的共享增加,这与早期的研究一致。
除了向成年人微生物菌群发展,我们还关注婴儿微生物功能的成熟。我们的结果强调了肠道微生物组在为发育中的婴儿生产必需氨基酸和维生素中发挥的作用。虽然婴儿肠道微生物群在出生4个月后获得了产生氨基酸和维生素的能力,但转运体能力的增加表明,新生儿的微生物组已经准备好迎接肠道环境即将发生的变化,并向成熟的方向发展。有趣的是,考虑到肠道微生物群可能影响行为的证据,发育中的肠道微生物组的许多功能与维生素、铁和氨基酸的代谢有关,这些物质也是大脑正常发育所必需的。因此增加了肠道微生物群可能影响行为的可能性。
我们的结果还强调了母乳喂养在生命第一年肠道微生物群落的形成和演替中的作用。不再母乳喂养的儿童肠道微生物群富含Clostridia ,这种物种在成人中很普遍,如Roseburia, Clostrium和Anaerostipes。相比之下,Bifidobacterium 和 Lactobacillus在12个月大的母乳喂养婴儿的肠道微生物群中仍然占主导地位。不同的微生物结构也与功能转变有关,因为固体食物的引入促进了多糖降解能力的提高,直到婴儿停止母乳喂养,这一点才变得明显。因此,我们的结果强烈表明停止母乳喂养而不是引入固体食物是向成人微生物群发展的主要驱动力。事实上,最近的研究表明母乳喂养的婴儿与成年微生物群落类型(即以Bacteroides为主)相关联,并与恒河猴(rhesus macaques)中明显的微生物群特征和Th17型免疫反应的扩展相关联。这些研究和我们的结果暗示了母乳喂养对肠道微生物组的终生影响,对代谢和免疫健康的可能影响我们才刚刚开始了解。
研究方法
研究人群和取样
Study Population and Sampling
作为更大研究的一部分,研究人群在到达产房前被招募,该研究得到了隆德地区伦理审查委员会的批准。获得了所有母亲的知情同意。获得了98份完整的婴儿/母亲样本。婴儿( 44名男孩 / 54名女孩)都是健康足月妊娠并且计划阴道分娩 (15名剖腹产,83名阴道分娩 ,两个阴道分娩的新生儿样本和一个剖腹产的新生儿样本缺失)。收集粪便样本,包括出生时的母亲和新生婴儿、4个月大(引入固体食物的时间)和12个月大(通常给儿童喂食全餐)的粪便样本,并记录喂养方式和抗生素的使用情况。进一步分析前,样品被冷冻在-80℃并储存。
DNA提取和宏基因组测序
DNA Extraction and Metagenomic Sequencing
按照制造商的说明书,使用(MACHEREY - NAGEL,德国)的NucleoSpin Soil kit从约100毫克粪便中分离基因组DNA,唯一的修改是使用FastPrep-24仪器( MP生物医学)以5.5 m/s的速度重复敲打珠粒60秒,以取代涡旋振荡。DNA文库的构建遵循制造商的说明( Illumina Hiseq2000 )。构建了一个插入大小为350 bp的成对末端文库,并对其进行了测序,每个末端有100 bp的读取长度。Adaptor污染、低质量reads和寄主污染读取已从原始测序reads中移除。平均每个样本产生3990万个高质量reads,用于进一步分析。来自每个样本的所有原始reads中,高质量reads的比例平均为86.7 %。
Contigs和基因组的重新组装
De Novo Assembly of Contigs and Genomes
我们使用SOAPdenovo2 将每个样品的高质量读数组合成contigs。对于每个样本,未比对(map)至NCBI数据库已知基因组的contig根据它们在样本间的协变量(covariations),使用排序列点鉴定簇结构(Ordering Points to Identify the Clustering Structure, OPTICS) 算法进行合并。然后每个bin,使用期望最大化 (expectation maximization,EM)算法优化,并根据GC含量对覆盖度的图表手动进行分类。使用SOAPdenovo2将每个bin的contigs组装成基因组。
构建MetaOTUs和分类
Construction of MetaOTUs and Taxonomic Assignments
根据基于MUMi的基因组-基因组距离和Spearman距离,来自NCBI的总共4356个重头组装(de novo assembled)的基因组草图(draft)和1147个细菌或古菌基因组在我们的样品中被检测到,并被聚类成MetaOTUs。对参数进行优化,使每个MetaOTU代表一个物种。
每个MetaOTU的分类学地位由位于MetaOTU内的NCBI基因组的分类学信息确定。
对于所有313个没有注释的MetaOTUs和373个已注释的MetaOTUs中的116个包含了新的组装的基因组,我们用在Rinke等人2013年的一篇文章描述的一个单拷贝保守基因数据集(a set of conserved single-copy genes,SCGs,139个细菌基因)和暗示了基因组完整性的139个细菌基因的覆盖度来分析。
对于包含来自新组装的基因组和来自NCBI参考基因组的116个MetaOTUs,对这些基因组分别进行统计分析。使用 PFAM 数据库的默认参数比对MetaOTUs中的非冗余基因与SCGs,如果基因与多个SCGs对齐,就采用分数最高的比对结果。
基因集构建和功能注释
Gene Catalog Construction and Functional Annotation
我们使用GeneMark v2.7从组装的contigs中进行基因预测。所有预测的基因使用BLAT 进行成对比对,其中长度超过90%可以与另一个contigs达到95 %以上的同一性的contig(不允许有缺口),会被当做冗余删除。我们分别为新生儿、4个月大婴儿、12个月大婴儿和母亲构建了四个基因集。
我们将非冗余基因翻译成预测的氨基酸序列,并用BLASTP (e值 ≤ 1e-5 )将这些基因与KEGG的一组蛋白质序列进行比对(版本59.0,去除了动物和植物序列)。每种蛋白质都被最高得分的注释分配给KO,包含至少一个超过60 bits的HSP得分。CAZy数据库中糖苷水解酶( glycoside hydrolases,GHs )和多糖裂解酶(polysaccharide lyases, PLs )的注释通过匹配KO结果中相应的酶( ECs )来进行。
根据他们的报告分数,从个体KOs的Z分数,鉴别出差异富集的KO通路、模块或CAZy家族。
分类注释和丰度计算
Taxonomic Annotation and Abundance Calculation
预测基因的分类信息是根据IMG数据库( v400 )使用先前详述的内部流程进行的,具体阈值是,70%的重叠和65%的相似度分配到门,85 %的相似度分配到属。一个分类单元的相对丰度是根据其基因的相对丰度来计算的。
生态学的参数
Ecological Parameters
根据Rao提出的方法,每个队列的MetaOTU或KO分布图的总多样性被分解为α-多样性(样本内)和β-多样性(样本间)。根据考虑了一个分类单元的出现(occurrence)和丰度(abundance)的IndVal值来识别特征属或MetaOTUs。
MetaOTU网络
MetaOTU Networks
Spearman的相关系数是根据阴道分娩婴儿每个阶段的丰度波动来计算的。新生儿和4个月之间或4个月和12个月之间变化的相互作用通过从一个阶段减去另一个阶段的系数来确定。如果在比较的两个阶段,MetaOTU在少于六个样本中出现,Spearman’s cc值 在-0.6和0.6之间,或者p≥0.05,都会被排除。置换检验(permutation)被执行了999次,以测试变化是否显著。测试统计数据中不低于原始观察数据的百分比是置换检验的P值。使用Cytoscape 3.0.2可视化MetaOTUs网络。
计算肠道菌群的年龄
使用R (3.0.1 )中的randomForest包中的默认参数,将每个训练样本( n = 49 )中所有MetaOTUs的相对丰度曲线与其相应的时间年龄(单位、天数)进行拟合,就像之前对来自16S焦磷酸测序的OTUs所做的那样。根据随机森林包中的rfcv函数,64个MetaOTUs的拟合度相当好,它们在置换重要性方面排名前64位。基于这64个MetaOTUs的随机模型随后被应用于测试样本( n = 15,21,9 ),以计算他们的“肠道微生物年龄”。年代年龄和肠道微生物年龄都是连续的数字,如Subramanian等人的结论一致。
译者简介
秋芒树,本科毕业于中国农业大学,硕士就读于英国帝国理工学院Computational Methods in Ecology and Evolution专业。关注婴儿肠道微生物,肠道细菌与噬菌体的相互作用。在宏基因组公众号发表《Nature:TEDDY计划中幼儿肠道微生物组随时间的发育》、《Cell子刊:成年同卵双胞胎的病毒组多样性与肠道微生物组多样性相关》、《CHM:新生儿肠道微生物菌群研究》 等。欢迎批评、指正和交流, j.wu18@imperial.ac.uk
翻译:秋芒树 英国帝国理工学院
责编:刘永鑫 中科院遗传发育所
拓展阅读
Temporal development of the gut microbiome in early childhood from the TEDDY study
https://www.nature.com/articles/s41586-018-0617-xRole of priority effects in the early-life assembly of the gut microbiota
https://www.nature.com/articles/nrgastro.2017.173Maternal gut and breast milk microbiota affect infant gut antibiotic resistome and mobile genetic elements
https://www.nature.com/articles/s41467-018-06393-w
Reference
Bäckhed F , Roswall J , Peng Y , et al. Dynamics and Stabilization of the Human Gut Microbiome during the First Year of Life[J]. Cell Host & Microbe, 2015, 17(5):690-703. https://www.cell.com/cell-host-microbe/fulltext/S1931-3128(15)00162-6













