多种机制抑制T细胞的功能,使其处于“失功能”状态。免疫检查点抑制剂,免疫调节剂等用于恢复免疫功能,重建免疫稳态。免疫活化阈值可用于衡量免疫活化状态及药物治疗效果。
阈值模型
大量的“正向”和“负向”因素,调节免疫系统,以实现免疫稳态。免疫调节在个体之间也有很大差异,并且可能是癌症免疫治疗患者差异结果和不良反应的主要因素之一。
阈值模型为理解免疫激活、自身免疫和抗肿瘤免疫提供了一个简单的参数,以便概念化免疫治疗的反应类型。
对于个体患者,绘制的水平线代表其免疫系统免疫激活的“阈值”。
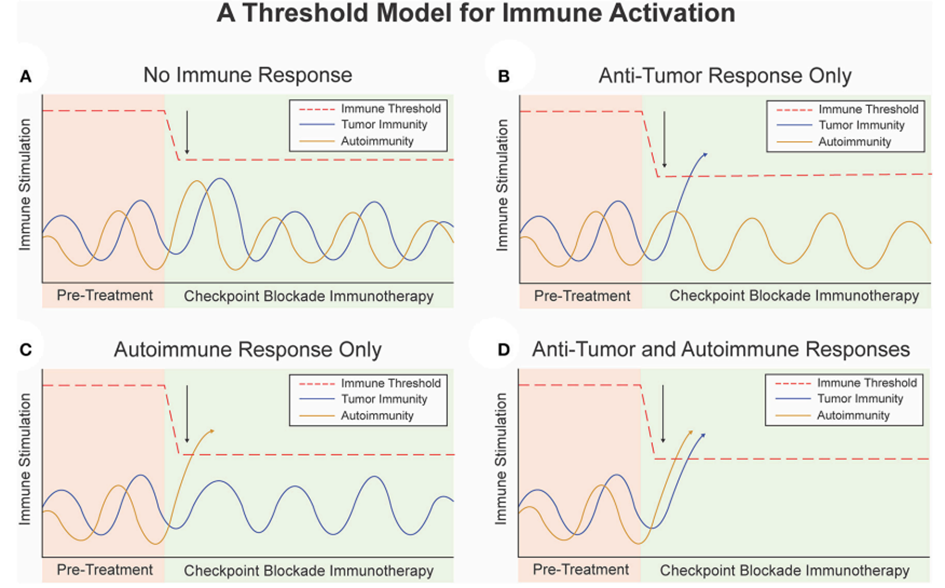
阈值表示引发免疫反应所需的免疫原性刺激水平,由免疫系统所有起作用的调节机制的总和决定。
免疫系统刺激低于该阈值,仍可能激活免疫系统的某些单个细胞,但不足以克服这些调节机制,产生有效的全身免疫反应。
在给定的患者中,有各种事件刺激或抑制其基线肿瘤或宿主免疫原性。我们可以将免疫原性水平随时间绘制为正弦“免疫原性曲线”,该曲线代表不同类型的基线免疫原性以及由于宿主和环境因素导致的基线肿瘤或宿主免疫原性的自然变化。这些曲线由多种因素决定,包括患者的遗传、环境暴露、健康、饮食以及正反馈和负反馈机制本身。
阈值模型的价值
解释自身免疫性疾病发病
遗传上易患自身免疫性疾病的人群,基线自身免疫原性曲线比没有这种风险因素的人具有更高的峰值。例如,在完全发病前,患有系统性红斑狼疮的患者可能存活多年,然后由于某些触发事件(比如感染)导致超过阈值,发展为完全成熟的自身免疫疾病。( Doria A, Canova M, Tonon M, Zen M, Rampudda E, Bassi N, et al. Infections as triggers and complications of systemic lupus erythematosus. Autoimmun Rev. (2008) 8:24–8. doi: 10.1016/j.autrev.2008.07.019)
机体保护性免疫发生
静息时,免疫原性曲线的峰值低于激活阈值,抗原特异性免疫应答不被促进。当免疫系统受到超过阈值水平的刺激时,例如由于细菌、病毒或其他外源性因子的存在,就会发生抗原特异性免疫反应。一旦超过阈值,正反馈回路和自分泌和旁分泌信号通路自然诱导抗原特异性T细胞或B细胞的快速扩增和繁殖。负调节机制仍然在调节这种反应的程度和持续时间方面发挥作用,并最终使免疫系统恢复到体内平衡或形成记忆反应的新基线。
肿瘤免疫疗法的成败
癌症免疫疗法的第一种方法是用细菌制剂增强对免疫系统,随后使用细胞因子或疫苗来驱动抗肿瘤免疫。这有效地增加了基线肿瘤免疫原性曲线的峰值,试图刺激超过阈值。然而,由于强大的负面调节机制,这种方法很少成功,并且在大多数情况下,免疫阈值可能高于单独使用这些激动剂可以达到的阈值。
与检查点阻断免疫疗法(CBI)一起使用的方法是直接抑制负调节机制,包括CTLA-4或PD-1 / PD-L等途径。这种方法有效地降低了免疫阈值,并减少了引发免疫反应所需的刺激量。双药检查点阻断将有效地进一步降低免疫激活的阈值。
单独单药检查点阻断的活性、客观反应、免疫毒性的发生,与双免疫检查点联合用药的显著增强,强烈支持这一阈值模型。
抗肿瘤免疫应答的激活,可能导致适应性耐药或出现试图破坏这种反应或有效地提高阈值的反调节机制。这可能对维持治疗,或在初始疗程后再次使用免疫检查点抑制剂产生不利影响。
过度激活的“副作用”
从该模型得出的另一个重要观点是,更多的刺激不一定对免疫反应更好。在许多情况下,过度刺激具有矛盾的反应,并导致抑制或活化诱导的细胞死亡。免疫系统必须不断尝试在激活(播散性感染的风险)和过度激活(自身免疫或细胞因子风暴的风险)下保持平衡。
因此,阈值模型还预测,在没有负调控(最低阈值)的情况下,只需要少量的正刺激即可引发免疫反应。这样做的临床意义是,在检查点抑制剂时代,在某些情况下可能需要更少的药物来最佳地诱导免疫反应。
参考资料
Bene, L.; Bagdány, M.; Damjanovich, L. T-cell Receptor Is a Threshold Detector: Sub- and Supra-Threshold Stochastic Resonance in TCR-MHC Clusters on the Cell Surface. Entropy 2022, 24, 389. https://doi.org/10.3390/e24030389
Guram K, Kim SS, Wu V, Sanders PD, Patel S, Schoenberger SP, Cohen EEW, Chen S-Y and Sharabi AB (2019) A Threshold Model for T-Cell Activation in the Era of Checkpoint Blockade Immunotherapy. Front. Immunol. 10:491. doi: 10.3389/fimmu.2019.00491
Sara Hamdan et al,Cytomegalovirus immune evasion sets the functional avidity threshold for protection by CD8 T cells,Medical Microbiology and Immunology (2023) 212:153–163 https://doi.org/10.1007/s00430-022-00733-w














