由于免疫检查点抑制剂(ICIs)在转移性RCC中已被证实有效,因此备受期待。III期KEYNOTE-564研究第一次期中分析达到了DFS主要终点,最终分析所需的事件数仅有33%,但在关键次要终点OS方面,帕博利珠单抗组有获益倾向。其他三个ICIs用于RCC围手术期的III期临床试验:IMmotion010(阿替利珠单抗辅助治疗),CheckMate-914(纳武利尤单抗联合或不联合伊匹木单抗辅助治疗),PROSPER(术前、术后使用纳武利尤单抗)却均未达到主要终点。
评价任何疾病的任何治疗是否有获益,都应该以它是否能提高生存率或生活质量来判断。对于癌症的辅助治疗,对总生存期(OS)的影响是至关重要的:如果能够改善长期预后,患者和他们的肿瘤医生或愿意接受明显的不良反应和短期内生活质量的下降。评价辅助治疗随机对照试验(RCT)的有效性,需要分析有关试验设计的几个重要问题(总结如下图):
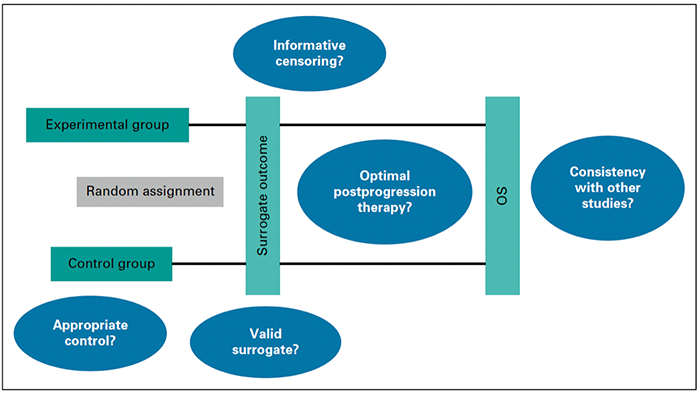
1、如果主要终点不是OS,那么它是否是OS的有效替代终点?无病生存期(DFS)一直是许多癌症类型辅助治疗试验的主要终点,但这一终点的改善可能和以下两个因素有关:更多的患者被治愈,或者是延迟复发但并没有改变长期生存率。
与随机分配接受辅助治疗的患者相比,对照组患者如果复发后使用相同的治疗方案,可能会抵消辅助治疗组的生存获益。在乳腺癌的辅助治疗试验中,2年DFS仅与(较小的)5年OS获益中度相关。通过一个对13项RCTs、共6400多名患者的分析,Harshman等人得出结论,肾癌辅助治疗5年DFS和5年OS率没有强相关性。部分学者可能认为延迟复发也是一种获益,即使后续OS没有改善。但是,这种获益可能被所有患者(包括那些没有复发的患者)接受辅助治疗的生理和经济毒性所抵消。
2、在使用替代终点的情况下,是否有证据表明结果存在偏倚(basis)?具体来说,如果主要终点是DFS,试验的两个组之间是否存在不同的患者丢失(loss),从而导致在记录疾病复发之前出现患者信息删失?信息删失会影响研究的随机化分配,并不是原始随机分组的代表性样本。
3、试验中的患者在疾病复发后是否接受了最佳治疗?如果对照组患者之后没有接受辅助治疗用药或类似的药物,该试验并不能证明在部分复发患者中,早期使用该药物作为辅助治疗比在复发后选择性使用该药物能提供更好的OS。
4、试验结果与评估相同或类似治疗的RCT结果的一致性如何?结果的一致性比单个试验中显著的P值更能显示出真实的结果。
接受手术的RCC患者应尽可能去除了所有可见的病变。多种预后模型根据肿瘤的临床特征估计了复发和死亡风险:被分类为高危的患者(如II期 [>7cm] 并有组织学类型不佳或周围组织受累,或淋巴结阳性),50%或更多的患者最终死于该疾病。因此,迫切需要有效的辅助治疗来提高生存率。Keynote-564研究比较了辅助治疗一年帕博利珠单抗和安慰剂,报告了其主要终点DFS的显著改善,HR为0.63(95% CI,0.50~0.80),且有OS获益趋势。这一结果导致FDA和EMA批准帕博利珠单抗的辅助治疗适应症,并被NCCN、ESMO和其他学术机构纳入指南,但我们认为这些决定可能为时过早。
结合上面所提出的有关研究设计的四个问题,Keynote-564研究存在所示每一个问题的影响。在随访的早期阶段,各研究组之间的脱落率不均匀,这提示数据丢失的原因并不是患者在数据锁定时仍在接受指定的治疗。我们缺乏关于这些删失患者复发的信息,但在敏感性分析中,我们构建了校正治疗失败时间(mTTF)的曲线,其中除疾病复发或死亡外,过多删失也被视为事件(见下图):mTTF的HR为0.81(95% CI,0.65~1.00),P=0.056。该研究的作者对DFS主要终点进行了敏感性分析,HR值仍旧显示获益,但他们没有进行mTTF评估。
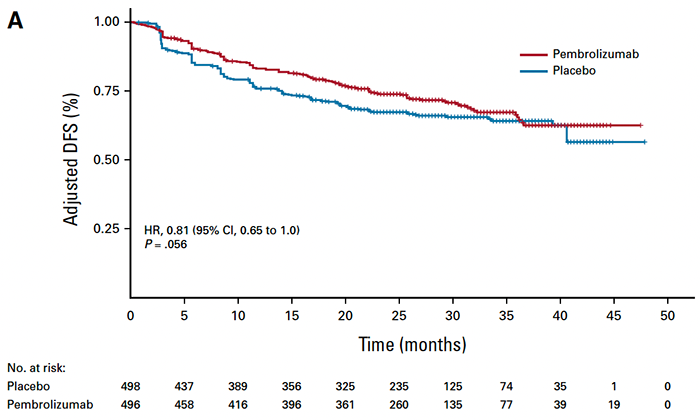
第二,在Keynote-564研究中复发患者接受的后续治疗可能是次优的。在对照组的166例复发患者中,只有36%接受了任何形式的免疫治疗,有一致性的证据表明,这种治疗可以提高转移性RCC的生存率。作者在文章中指出,肾切除术后复发患者的标准治疗是多种多样的,可能包括密切监测、局部消融治疗、手术或靶向治疗,84%复发的对照组患者有转移。中位随访时间为30个月,很少有缓慢进展的复发患者,对于大多数复发患者,最佳治疗包括免疫治疗。在一些国家,由于治疗费用等问题,晚期患者可能无法接受免疫治疗。如果Keynote-564研究中OS“small”显著的差异随着随访时间的延长可能会更加更明显,这可能是由于复发时对照组的治疗较差,而不是随机分配接受辅助帕博利珠单抗患者的治疗更好。
最后,另外3项评估纳武利尤单抗+伊匹木单抗或阿替利珠单抗辅助免疫治疗RCC的试验结果已经发表,这些试验均未显示DFS或OS的显著差异。有些人可能会认为帕博利珠单抗是一种更有效的药物,但这并没有得到全部支持。有学者提出,这些不同的结果可能是由于试验设计的差异,例如入组的患者特征,辅助治疗的持续时间等。但是总的来说,上述几项试验之间的患者差异并不大,3个阴性试验DFS曲线提示,随机分组之间的删失率没有显著差异,这与Keynote-564研究似乎不同。即使没有固有偏倚,由于统计存在的可变性,即使评估相似设计的试验也会得出不同的结果。有专家曾经说:不可复制率较高(缺乏证实)的研究是容易形成的。然而,仅根据一项具有统计显著性(常为P<0.05)的研究来宣称结论性发现的策略理由并不充分。
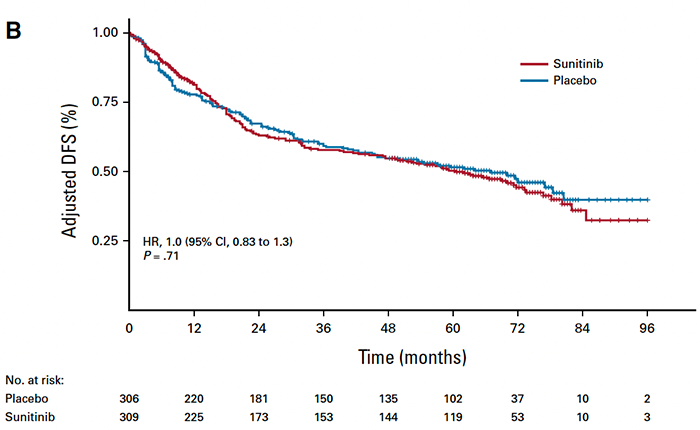
目前,在部分指南中,包括NCCN和ESMO的指南,都建议对高风险RCC使用辅助帕博利珠单抗治疗,但欧洲泌尿协会(适当地,appropriately)认为获益的证据并不强。基于上述讨论的内容,我们认为高危RCC患者肾切除术后使用帕博利珠单抗或其他辅助治疗的作用尚未得到证实,期待OS结果明确有实质性的改善。同样的,未来的辅助治疗试验应避免图中总结的问题,将OS作为主要终点,并给对照组复发患者提供最佳治疗。
参考文献
J Clin Oncol. 2023 Mar 24; JCO2300280. doi: 10.1200/JCO.23.00280.














