1963年,Christian de Duve首次提出了自噬(Autphagy)的概念,该词源自希腊语:“auto”表示自我,“phagy”表示进食,合起来就是“自己吃自己”的意思。
它描述了真核生物细胞中双层膜囊泡将胞内成分包裹起来并将它们运输到溶酶体进行降解的现象。在接下来的二十年,由于技术限制自噬研究领域进展缓慢,并未引起广泛关注。
直到1990年,Yoshinori Ohsumi的出现。
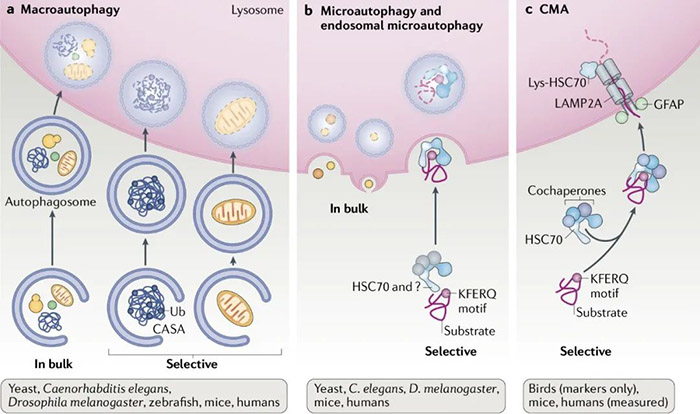
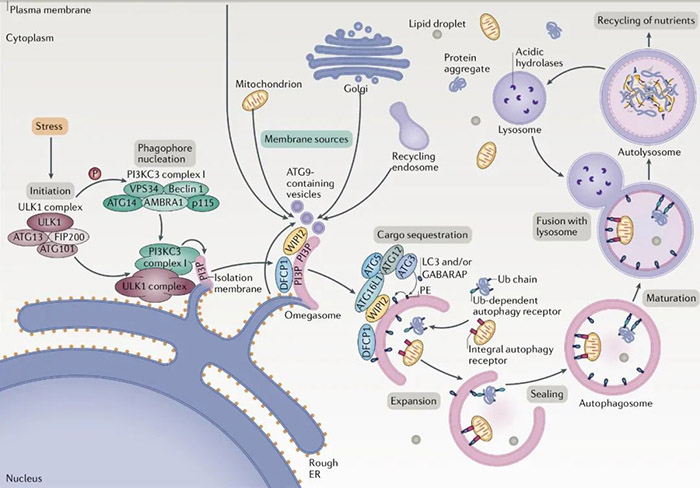
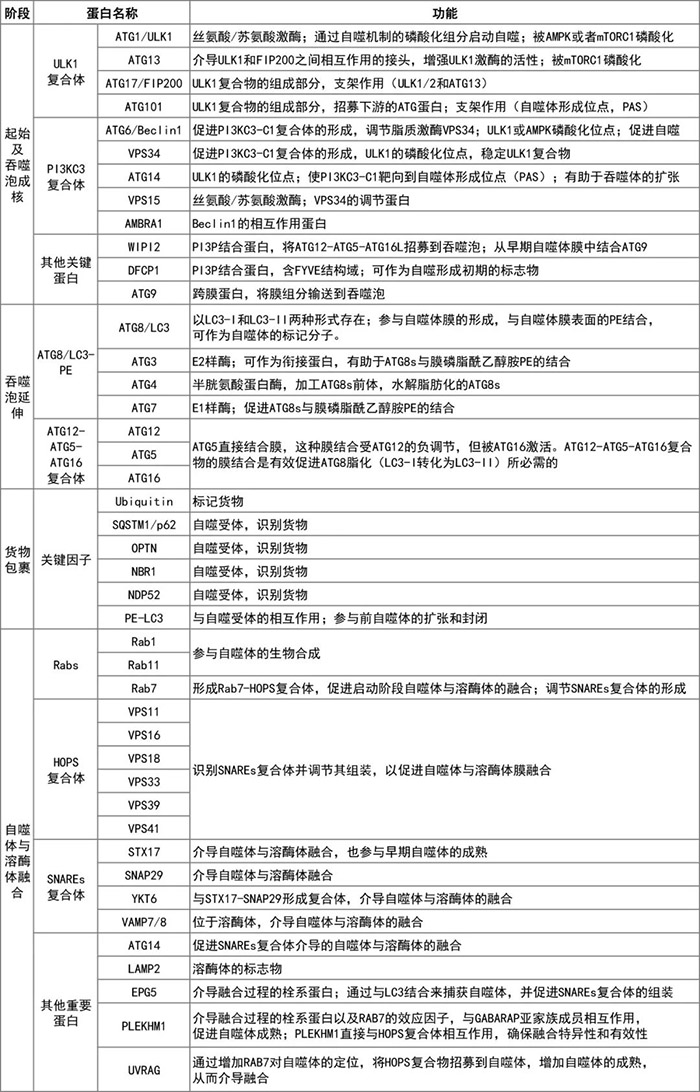
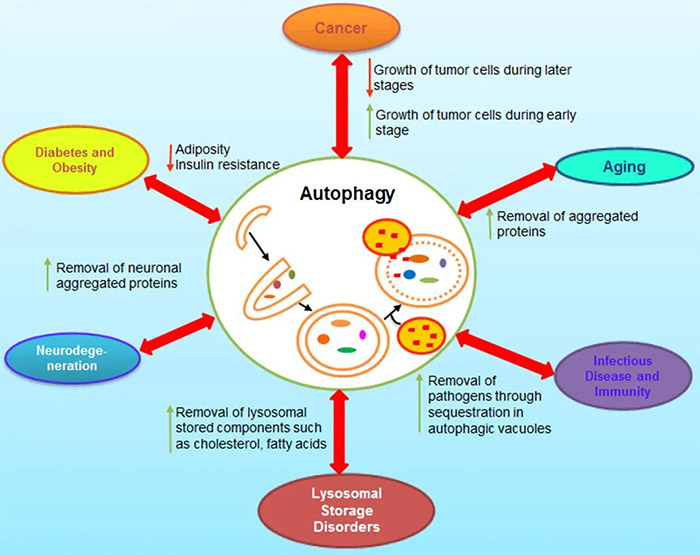
(图源:https://www.titech.ac.jp/nobel) Yoshinori Ohsumi是一名日本科学家,现任职于东京工业大学。他用一系列严谨的科学实验在酿酒酵母中直观地展现了细胞自噬现象,发现并克隆了多个自噬关键基因,阐明了酵母中的自噬机制;并展示了在人的细胞中也有相似的复杂机制,极大地促进了自噬研究的发展。 2003年,Daniel Klionsky等人将这些基因命名为ATG(AuTophaGy)基因,并研究了它们编码的蛋白质与其在自噬中的功能之间的相互作用;2005年,Daniel Klionsky出版并主编了新期刊《Autophagy》,PubMed上发表的自噬研究论文数量也逐年增加;2016年,Yoshinori Ohsumi因发现自噬机制而获得诺贝尔医学或生理学奖。 自此,自噬越来越受到关注,已成为生物学、医学、植物学和微生物学的超级热门研究领域。 今天小P就带领大家了解一下细胞自噬相关知识,各位看官坐稳咯~ 自噬的定义和分类 1.自噬的定义 自噬是真核生物中一种进化上高度保守的、用于降解和回收利用细胞内生物大分子和受损细胞器的过程;其完成依赖于正常的溶酶体功能。 自噬能够清除细胞内错误折叠的蛋白和受损及衰老的细胞器,将其降解产生能量和小分子,如氨基酸等供细胞再次利用,这对细胞耐受不良环境、维持内稳态十分重要;是细胞的一种自我保护机制,也与多种生理和病理进程相关。 2.自噬的分类 根据细胞物质通向溶酶体途径的不同,自噬一般分为三类:巨自噬 (macroautophagy)、微自噬(microautophagy)和分子伴侣介导的自噬(chaperone-mediated autophagy)。 巨自噬其特征是双层膜结构“自噬体”的形成,自噬体包裹胞质成分,如蛋白质聚集体、损伤或衰老的线粒体、过氧化物酶体等,最终与溶酶体融合。 微自噬则是溶酶体直接内陷成囊泡,包裹部分胞质进入溶酶体,没有独立的双层膜自噬体形成。 分子伴侣介导的自噬则不依赖囊泡结构,直接借助伴侣蛋白Hsc70,特异性地降解带有独特识别五肽基序(KFERQ样)的靶蛋白,溶酶体膜上的受体蛋白LAMP2A识别结合蛋白暴露的KFERQ基团,引导靶蛋白进入溶酶体降解,具有高度选择性。 当然,部分巨自噬和微自噬也会对“货物”有选择性,比如Cvt途径、过氧化物酶体自噬和线粒体自噬、内质网自噬等。这些选择性自噬的主要过程与非选择性自噬基本类似,但选择性自噬有自己特异的受体蛋白介导特定的包含物配体,即有识别底物的过程。 图源[1]:https://www.nature.com/articles/s41580-018-0001-6 此外,据细胞所处环境及自噬发生的程度不同,细胞自噬还可分为基础自噬和诱导自噬。基础自噬是一种在大多数细胞中持续发生而水平相对较低的细胞自噬过程,对细胞内物质的更新及内稳态的维持具有不可或缺作用;诱导自噬则属于一种应激状态,其发生程度明显强烈,在细胞应对外界恶劣环境、维持生存中发挥重要功能。 自噬的过程与关键自噬蛋白 1.自噬的过程 巨自噬作为经典的细胞自噬,也是过程最复杂的一种自噬。其发现最早,机制研究最清晰,因此也被狭义的等同为细胞自噬,下文中的自噬不作特别说明即为巨自噬。其发生可分为以下几个阶段: 1)自噬诱导阶段(Induction):主要通过ATG1/ULK1复合体(包括ATG1/ULK1、ATG13、FIP200和ATG101)来介导。在营养丰富的条件下,雷帕霉素靶蛋白复合物1(mTORC1)与ATG1/ULK1复合物结合,会磷酸化ATG1/ULK1和ATG13,导致它们失活,抑制自噬发生。当缺乏营养或用雷帕霉素(Rapamycin,mTORC1复合物抑制剂)处理时,mTORC1从复合物中解离,ATG1/ULK1和ATG13磷酸化水平降低,ATG1/ULK1复合物形成,自噬启动。(注:ATG1即Yoshinori Ohsumi发现并命名的第一个酵母自噬相关基因,ULK1是哺乳动物中ATG1的同源蛋白。) 2)前体成核阶段(Nucleation):主要由Vps34-Beclin 1复合体介导,该复合物由Vps34(PIK3C3)、Beclin 1(ATG6)、Vps15(PIK3R4或p150)和ATG14组成,可生成Ptdins3P,招募其他效应蛋白,介导吞噬泡成核;还可召集ATG12-ATG5-ATG16复合物以及LC3,并通过后两者促进吞噬泡膜的延伸。 3)延伸阶段(Elongation):自噬前体形成之后,吞噬泡膜会继续延伸,直至完全包裹内容物。在此过程中,两个泛素样蛋白(UBL)修饰系统发挥关键作用。 第一个是ATG5-ATG12复合体。ATG12作为类泛素蛋白,在ATG7(类E1泛素活化酶)和ATG10(类E2泛素转移酶)的作用下,结合ATG5,生成ATG12-ATG5复合物。随后该复合物又与ATG16结合形成ATG12-ATG5-ATG16复合物,该复合物具有类E3泛素连接酶活性。 第二个是ATG8/LC3系统。ATG8(LC3)作为泛素样蛋白,首先被半胱氨酸蛋白酶ATG4切割成胞浆可溶性的LC3-I,然后被ATG7(类E1酶)激活处理,在ATG3(类E2酶)和ATG12-ATG5-ATG16复合物的作用下,最后与脂质磷脂酰乙醇胺(PE)共价结合,形成脂溶性的LC3-PE(LC3-II),参与自噬体的延伸。 4)自噬体成熟阶段:随着自噬体的扩张和封闭,自噬体经历成熟过程,包括逐渐清除在自噬体外膜上的ATGs蛋白,招募负责溶酶体传递的蛋白和介导与溶酶体融合的蛋白。 5)自噬体与溶酶体融合阶段(Fusion):自噬体与溶酶体融合,首先自噬体外膜与溶酶体膜融合,形成自噬溶酶体(autolysosome)。随后自噬体内膜和内容物被溶酶体内的脂酶和蛋白酶降解为小分子,被细胞重新利用。细胞骨架成分和相关的运动蛋白,栓系因子(Tethering factors),磷脂和特定的SNAREs复合物,已经被确定为确保精确和有效融合的重要角色。 图源[2]:https://www.nature.com/articles/s41580-018-0003-4 2.关键自噬蛋白 自噬的发生过程,需要多种自噬相关蛋白的参与。目前已有大约40个自噬相关基因被发现,他们在酵母中和哺乳动物中高度保守,各自在自噬过程中发挥重要作用。当然细胞自噬的研究还在火热进行中,相信未来还会有更多的ATG基因被发现。 参考[2]:https://www.nature.com/articles/s41580-018-0003-4 自噬与疾病 真核细胞中物质的分解代谢主要有两种途径:泛素-蛋白酶体途径和细胞自噬途径。其中泛素蛋白酶体途径主要是选择性地降解细胞内的短效蛋白质;而自噬途径则主要负责细胞内的长效大分子及受损细胞器的降解和回收。正常的细胞自噬过程对细胞内稳态的维持以及细胞生命活动的顺利进行十分重要。 许多疾病的发生,都与细胞自噬密切相关。包括癌症、神经退行性疾病、心血管疾病、炎症与免疫反应、发育和衰老等。研究人员也都在积极探索自噬与人类各种病理生理状态之间的关系,并正在研究各种疾病中自噬调控的分子机制,通过抑制或促进自噬来减缓疾病进展,为许多疾病的靶向治疗提供了非常有前景的新思路。 图源[3]:https://doi.org/10.1016/j.biopha.2018.05.007 1.自噬与癌症 癌症是第一个被发现与自噬功能受损有关的疾病,二者间的联系也是当今自噬研究中的一个重要内容。 在肿瘤起始和恶性转化过程中,自噬被认为是一种抑癌机制。它通过清除受损的细胞和细胞器来限制细胞增殖和基因组的不稳定性。早期有报道显示,功能获得性突变的抑癌基因P53通过Akt/mTOR通路抑制自噬产生,进而调节癌症的进展[4]。1999年Levine团队鉴定了酵母ATG6的哺乳动物同源物Beclin 1,并证明了Beclin 1的肿瘤抑制作用;据观察Beclin1基因在卵巢癌中缺失率高达75%,在乳腺癌中缺失率高达50-70%[5]。 然而,也有研究显示自噬有促癌作用。高速生长的癌细胞需要物质和能量基础,同时也需要抵御来自免疫系统的攻击,在这个过程中,部分研究显示自噬成为了癌细胞生长的一个助力。有证据显示,在使用顺铂药物治疗舌鳞状细胞癌时,自噬的激活会促进癌细胞存活,自噬的抑制则会增加肿瘤细胞的敏感性[6]。在Jingfang Ju等人的研究中,miRNA-502在HCT-116细胞中的异位表达中断了急性和长期营养饥饿下的自噬通量,并显著降低了结肠癌细胞的生长;同时miRNA-210和124等可以通过诱导自噬而促进癌症发展和提供化疗耐药性[7]。 由此可见,在不同的环境因素或稳定状态下,自噬既可以阻止也可以促进肿瘤的发生。 2.自噬与衰老 细胞内损伤物质的积累是所有衰老细胞的普遍特征,能导致细胞内稳态的紊乱,细胞生存能力降低。而细胞自噬则是细胞内主要的分解代谢途径,显然细胞自噬与衰老之间存在着密切联系。 有研究显示,口服亚精胺可以延长小鼠寿命,防止衰老小鼠心肌肥大,保护其心肌舒张功能;并且显著增强小鼠心脏自噬和线粒体自噬水平;而亚精胺对ATG5基因敲除小鼠则没有这种心脏保护作用[8]。敲除自噬相关基因ATG7、ATG4和ATG9,植物能正常生长,但是却加速叶片衰老[9]。与青年人比较,在健康的长寿老人中Beclin 1水平增高[10]。 这些证据都表明了自噬在衰老进程中的重要功能,为人类长寿的机制突破提供了理论基础。 3.自噬与神经退行性疾病 大脑是人体的高能耗器官,脑组织需要大量能量用于生物合成和新陈代谢。机体衰老之后的代谢降低可导致大脑认知功能的衰退,这也是神经退行性疾病的一个重要危险因素。 阿兹海默症(AD)的一个关键病理特征就是神经元细胞内异常的Aβ1-42蛋白聚集。有研究表示衰老机体自噬标志物LC3表达减少,自噬水平下降,导致Aβ1-42蛋白沉积增加;提高机体自噬水平则可减少Aβ1-42蛋白沉积,延缓认知功能障碍[11]。Spilman等提出,雷帕霉素可能通过阻断mTOR对FoxO3的抑制,激活自噬,延缓AD小鼠的认知功能障碍[12]。 由此可见,自噬的激活在神经退行性疾病的进展当中也是发挥了关键作用,通过提高自噬水平来特异性清除神经元中过量积累的毒蛋白或许可以为此类疾病的治疗提供一个可行思路。 4.自噬与免疫 自噬作为目前发现的唯一一种可以降解细胞器和较大蛋白聚集物的途径,因此也被预测可能参与外来微生物的降解过程。许多研究都证实了这一点,自噬可以用于清除细胞内的细菌和病毒等微生物。 A族链球菌(GAS)是可以侵入非吞噬细胞的主要人类病原体之一。进入到细胞质中的A族链球菌会被自噬体选择性捕获,运送至溶酶体进行降解[13]。同时,细胞自噬途径将其降解产物提呈给NKT等固有免疫细胞,也能够活化T细胞等适应性免疫细胞。一些病毒和细菌抗原在经过自噬溶酶体处理后,被呈递到MHCⅡ分子上,如人类肿瘤病毒爱泼斯坦巴尔病毒(EBV)的核抗原1(EBNA1)[14]。 当然,除清除病原体和抗原提呈外,细胞自噬还会在维持免疫细胞增殖和存活中发挥作用,多层次参与到免疫反应当中。