前面我们谈到了来自基因组暗物质神秘的非编码长链RNA(lncRNA)、非编码环形RNA(ciRNA)、微小的RNA(miRNA),现在我们再来谈谈与微小的RNA(miRNA)有密切关系的小干扰RNA(siRNA)和短发夹RNA(shRNA)。介绍他们之前我们需要先了解下RNA干扰(RNAi)技术。
RNA干涉(RNAinterference,RNAi)是有效沉默或抑制目标基因表达的过程,指内源性或外源性双链RNA(dsRNA)介导的细胞内mRNA发生特异性降解,从而导致靶基因的表达沉默,产生相应的功能表型缺失的现象。RNA干扰由转运到细胞细胞质中的双链RNA激活。沉默机制可导致由小干扰RNA(siRNA)或短发夹RNA(shRNA)诱导实现靶mRNA的降解,或者通过小RNA(miRNA)诱导特定mRNA翻译的抑制。通过短反义核酸(siRNA和shRNA序列)锁定细胞mRNA,从而实现其随后的降解。这反过来阻断了该蛋白的进一步表达/聚集,导致其水平的下降,最终实现抑制作用。
RNA干扰最初是怎样发现的呢?我们也简单回顾下:
早在1984年人们就发现反义RNA能够抑制基因的表达,但后来人们发现发现双链RNA在抑制基因表达方面实际上比单链RNA更有效。RNA干扰现象是1990年由约根森(Jorgensen)研究小组在研究查尔酮合成酶对花青素合成速度的影响时所发现的,为得到颜色更深的矮牵牛花而过量表达查尔酮合成酶,结果意外得到了白色和白紫杂色的矮牵牛花,并且过量表达查尔酮合成酶的矮牵牛花中查尔酮合成酶的浓度比正常矮牵牛花中的浓度低50倍。约根森推测外源转入的编码查尔酮合成酶的基因同时抑制了花中内源查尔酮合成酶基因的表达。1992年,罗马诺(Romano)和Macino也在粗糙链孢霉中发现了外源导入基因可以抑制具有同源序列的内源基因的表达。1995年,Guo和Kemphues在线虫中也发现了RNA干扰现象。1998年,安德鲁·法厄(Andrew Z. Fire)等在秀丽隐杆线虫(C.elegans)中进行反义RNA抑制实验时发现,作为对照加入的双链RNA相比正义或反义RNA显示出了更强的抑制效果。从与靶mRNA的分子量比考虑,加入的双链RNA的抑制效果要强于理论上1:1配对时的抑制效果,因此推测在双链RNA引导的抑制过程中存在某种扩增效应并且有某种酶活性参与其中。并且将这种现象命名为RNA干扰。
RNA干涉(RNAi)在实验室中是一种强大的实验工具,利用具有同源性的双链RNA(dsRNA)诱导序列特异的目标基因的沉寂,迅速阻断基因活性。siRNA在RNA沉寂通道中起中心作用,是对特定信使RNA(mRNA)进行降解的指导要素。siRNA是RNAi途径中的中间产物,是RNAi发挥效应所必需的因子。
siRNA和shRNA的作用机制
两个在RNAi途径的基因沉默中具有实质利害关系的是双链小干扰RNA(siRNA)和基于载体的短发夹RNA(shRNA)。虽然siRNA和shRNA(图1)都可用于蛋白沉默,但它们的作用机制有所不同(图2)。不管是长的双链RNA还是短的约21bp碱基对的双链都能够直接被转运到组织培养的细胞中。虽然有一些报道提到siRNA在转染细胞时是被转运到细胞核中的,但更普遍的看法是它们在细胞质中聚集。长的双链RNA与Dicer一起形成复合物,双链特异性的核糖核酸酶III能够将它们处理成带有两个游离碱基的长度为21-23nt的siRNA。随后这些siRNA片段与RISC结合,RISC由Argonaute-2(Ago-2)、Dicer和TAR-RNA-结合蛋白(TRBP)组成。然后RNA的两条链分开,其中一条链从复合物上分离。5'端双链稳定性最低的那条链被选择出来,稳定的并入沉默复合物中。shRNA在转染/转导细胞的细胞核中的合成,形成发夹结构,茎区成对的反义和正义链与未配对的成环核苷酸连接在一起(图1b和1c)。通过与miRNA的加工相同的RNAi机制,shRNA被加工成siRNA。使用细菌或病毒载体,shRNA被导入靶细胞的细胞核内,在某些情况下,载体可以稳定地整合到基因组中。根据驱动表达的启动子的不同,shRNA可被RNA聚合酶II或者III催化转录。在被Exportin-5转运到细胞质之前,这些初始的前体结构需要首先用Drosha及其双链RNA结合伴侣DGCR8加工形成pre-shRNA。pre-shRNA随后被Dicer和TRBP/PACT酶切,去除发卡结构,产生在两个3‘末端带有两个游离碱基的20-25nt的双链siRNA。这一有活性的siRNA随后被整合到沉默复合物上去。
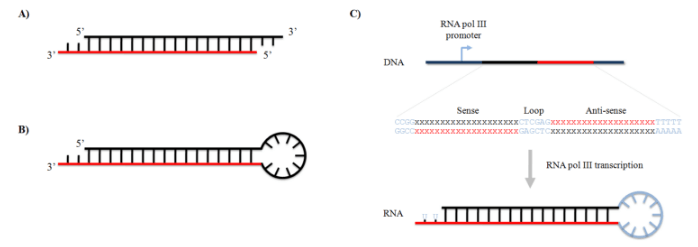
图1.siRNA和shRNA结构。
(A)siRNAs是短的RNA双链,在3‘端有两个碱基的游离。
(B)shRNA由正义链和反义链通过环状序列隔开共同组成。
(C)shRNA 构建用于插入表达载体。
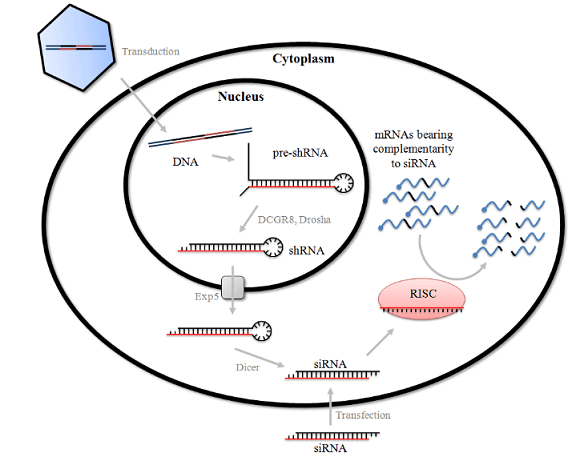
图2.RNAi介导的基因沉默机制。
在细胞核表达后,shRNA被Drosha加工然后由Exportin-5蛋白转运到细胞质中,在细胞质中它们与Dicer结合去除环状序列。在这一点上,它们与siRNA的加工方式(以短的双链形态导入细胞,然后被Dicer识别)相同。在与RISC结合并去掉其中一条RNA链后,它们识别mRNA占有互补序列,导致其降解。
一旦被整合到RISC后,shRNA和siRNA识别靶mRNA和降解的过程基本上是相同的。作为RISC的一部分,siRNA通过碱基互补配对以序列特异性的方式结合到靶mRNA,从而利用Ago-2的核酸酶H样活性裂解靶RNA的双链中心附近的磷酸骨架。某些生物的这个系统有一个有趣的特点,siRNA与靶mRNA的退火使siRNA作为引物,而靶mRNA作为依赖于RNA的RNA聚合酶的模板。这就合成出一个新的双链RNA,然后由Dicer酶加工,形成正反馈循环,增加了siRNA的量。应当指出的siRNA通常需要完全同源才能诱导降解。
miRNA与siRNA的相同点和区别
miRNA与siRNA之间有许多相同之处:
1.二者的长度都约在22nt左右。
2.二者都依赖Dicer酶的加工,是Dicer的产物,所以具有Dicer产物的特点。
3.二者生成都需要Argonaute家族蛋白存在。
4.二者都是RISC组分,所以其功能界限变得不清晰,如二者在介导沉默机制上有重叠。
5.miRNA和siRNA合成都是由双链的RNA或RNA前体形成的。
miRNA与siRNA的不同点:
1.根本区别是miRNA是内源的,是生物体的固有因素;而siRNA是人工体外合成的,通过转染进入人体内,是RNA干涉的中间产物。
2.结构上,miRNA是单链RNA,而siRNA是双链RNA。
3.Dicer酶对二者的加工过程不同,miRNA是不对称加工,miRNA仅是剪切pre-miRNA的一个侧臂,其他部分降解;而siRNA对称地来源于双链RNA的前体的两侧臂。
4.在作用位置上,miRNA主要作用于靶标基因3′-UTR区,而siRNA可作用于mRNA的任何部位。
5.在作用方式上,miRNA可抑制靶标基因的翻译,也可以导致靶标基因降解,即在转录水平后和翻译水平起作用,而siRNA只能导致靶标基因的降解,即为转录水平后调控。
6.miRNA主要在发育过程中起作用,调节内源基因表达,而siRNA不参与生物生长,是RNAi的产物,原始作用是抑制转座子活性和病毒感染。
RNAi 技术要点
1.siRNA 的设计
RNAi 技术要求siRNA 反义链与靶基因序列之间严格的碱基配对, 单个碱基错配就会大大降低沉默效应, 而且siRNA 还可以造成与其具同源性的其它基因沉默(也叫交叉沉默) , 所以在siRNA 的设计中序列问题是至关重要的。要求所设计的siRNA 只能与靶基因具高度同源性而尽可能少的与其他基因同源。设计siRNA 序列应注意以下几点: ①从靶基因转录本起始密码子AUG 开始, 向下游寻找AA 双核苷酸序列, 将此双核苷酸序列和其下游相邻19 个核苷酸作为siRNA 序列设计模板; ②每个基因选择4~5 个siRNA 序列, 然后运用生物信息学方法进行同源性比较, 剔除与其他基因有同源性的序列, 选出一个特异性最强的siRNA; ③尽量不要以mRNA 的5'端和3'端非翻译区及起始密码子附近序列作为设计siRNA的模板, 因为这些区域有许多调节蛋白结合位点(如翻译起始复合物) , 调节蛋白会与RISC 竞争结合靶序列, 降低siRNA 的基因沉默效应。
2.siRNA 的合成
目前获得siRNA 主要有体外制备和体内表达两种方式。
2.1.体外制备
2.1.1.化学合成
许多公司都可以根据用户要求提供高质量的化学合成siRNA。主要的缺点包括价格高,定制周期长,特别是有特殊需求的。由于价格比其他方法高,为一个基因合成3—4对siRNAs 的成本就更高了,比较常见的做法是用其他方法筛选出最有效的序列再进行化学合成。
最适用于:已经找到最有效的siRNA的情况下,需要大量siRNA进行研究
不适用于:筛选siRNA等长时间的研究,主要原因是价格因素
2.1.2.体外转录
以DNA Oligo为模版,通过体外转录合成siRNAs,成本相对化学合成法而言比较低,而且能够比化学合成法更快的得到siRNAs。不足之处是实验的规模受到限制,虽然一次体外转录合成能提供足够做数百次转染的siRNAs,但是反应规模和量始终有一定的限制。而且和化学合成相比,还是需要占用研究人员相当的时间。值得一提的是体外转录得到的siRNAs毒性小,稳定性好,效率高,只需要化学合成的siRNA量的1/10就可以达到化学合成siRNA所能达到的效果,从而使转染效率更高。
最适用于:筛选siRNAs,特别是需要制备多种siRNAs,化学合成的价格成为障碍时。
不适用于:实验需要大量的,一个特定的siRNA。长期研究。
2.1.3.用RNase III 消化长片断双链RNA制备siRNA
其他制备siRNA的方法的缺陷是需要设计和检验多个siRNA序列以便找到一个有效的siRNA。而用这种方法——制备一份混合有各种siRNAs “混合鸡尾酒” 就可以避免这个缺陷。选择通常是200—1000碱基的靶mRNA模版,用体外转录的方法制备长片断双链dsRNA ,然后用RNase III (or Dicer) 在体外消化,得到一种siRNAs“混合鸡尾酒”。在除掉没有被消化的dsRNA后,这个siRNA混合物就可以直接转染细胞,方法和单一的siRNA转染一样。由于siRNA混合物中有许多不同的siRNAs,通常能够保证目的基因被有效地抑制。
dsRNA消化法的主要优点在于可以跳过检测和筛选有效siRNA序列的步骤,为研究人员节省时间和金钱(注意:通常用RNAse III通常比用Dicer要便宜)。不过这种方法的缺点也很明显,就是有可能引发非特异的基因沉默,特别是同源或者是密切相关的基因。现在多数的研究显示这种情况通常不会造成影响。
最适用于:快速而经济地研究某个基因功能缺失的表型
不适用于:长时间的研究项目,或者是需要一个特定的siRNA进行研究,特别是基因治疗
在体外(in vit ro) 可用不同的方法将siRNA导入靶细胞, 一般来讲化学合成和体外转录合成的siRNA 可用电转移(elect roporation) 、微注射和转染的方法引入细胞。而表达质粒则常通过转染的方法导入靶细胞然后再表达siRNA。向体内(in vivo) 导入siRNA 的研究工作也已有报道, 如有研究者用静脉注射的方法将合成的siRNA 引入动物体内进行基因功能的研究。
2.2体内表达
前面的3种方法主要都是体外制备siRNAs,并且需要专门的RNA转染试剂将siRNAs转到细胞内。而采用siRNA表达载体和基于PCR的表达框架则属于:从转染到细胞的DNA模版中在体内转录得到siRNAs。这两种方法的优点在于不需要直接操作RNA。
2.2.1.siRNA表达载体
多数的siRNA表达载体依赖三种RNA聚合酶III 启动子(pol III)中的一种,操纵一段小的发夹RNA(short hairpin RNA, shRNA)在哺乳动物细胞中的表达。这三类启动子包括大家熟悉的人源和鼠源的U6启动子和人H1启动子。之所以采用RNA pol III启动子是由于它可以在哺乳动物细胞中表达更多的小分子RNA,而且它是通过添加一串(3到6个)U来终止转录的。要使用这类载体,需要订购2段编码短发夹RNA序列的DNA单链,退火,克隆到相应载体的pol III 启动子下游。由于涉及到克隆,这个过程需要几周甚至数月的时间,同时也需要经过测序以保证克隆的序列是正确的。siRNA表达载体的优点在于可以进行较长期研究——带有抗生素标记的载体可以在细胞中持续抑制靶基因的表达,持续数星期甚至更久。
病毒载体也可用于siRNA表达,其优势在于可以直接高效率感染细胞进行基因沉默的研究,避免由于质粒转染效率低而带来的种种不便,而且转染效果更加稳定。
最适用于:已知一个有效的siRNA序列,需要维持较长时间的基因沉默。
不适用于:筛选siRNA序列(其实主要是指需要多个克隆和测序等较为费时、繁琐的工作)。
2.2.2. siRNA表达框架
siRNA表达框架(siRNA expression cassettes,SECS)是一种由PCR得到的siRNA表达模版,包括一个RNA pol III启动子,一段发夹结构siRNA,一个RNA pol III终止位点,能够直接导入细胞进行表达而无需事前克隆到载体中。和siRNA表达载体不同的是,SECs不需要载体克隆、测序等颇为费时的步骤,可以直接由PCR得到,不用一天的时间。因此,SECs成为筛选siRNA的有效工具,甚至可以用来筛选在特定的研究体系中启动子和siRNA的最适搭配。如果在PCR两端添加酶切位点,那么通过SECs筛选出的最有效的siRNA后,可以直接克隆到载体中构建siRNA表达载体。构建好的载体可以用于稳定表达siRNA和长效抑制的研究。
这个方法的主要缺点是①PCR产物很难转染到细胞中②不能进行序列测定,PCR和DNA合成时可能差生的误读不能被发现导致结果不理想。
最适用于:筛选siRNA序列,在克隆到载体前筛选最佳启动子
不适用于:长期抑制研究。(如果克隆到载体后就可以了)
RNA干扰(RNAi)技术的应用
RNAi在基因沉默(silent gene)方面具有高效性和简单性,所以是基因功能研究的重要工具。大多数药物属于标靶基因(或疾病基因)的抑制剂,因此RNAi 模拟了药物的作用,这种功能丢失(LOF)的研究方法比传统的功能获得(GOF)方法更具优势。因此, RNAi 在今天的制药产业中是药物靶标确认的一个重要工具。同时,那些在靶标实验中证明有效的siRNA/shRNA本身还可以被进一步开发成为RNAi药物。
在药物标靶发现和确认方面,RNAi技术已获得了广泛的应用。生物技术公司或制药公司通常利用建立好的RNAi文库来引入细胞,然后通过观察细胞的表型变化来发现具有功能的基因。如可通过RNAi文库介导的肿瘤细胞生长来发现能抑制肿瘤的基因。一旦所发现的基因属于可用药的靶标(如表达的蛋白在细胞膜上或被分泌出细胞外),就可以针对此靶标进行大规模的药物筛选。此外,被发现的靶标还可用RNAi技术在细胞水平或动物体内进一步确认。
在疾病治疗方面,双链小分子RNA或siRNA已被用于临床测试用于几种疾病治疗,如老年视黄斑退化、肌肉萎缩性侧索硬化症、类风湿性关节炎、肥胖症等。在抗病毒治疗方面,帕金森病等神经系统疾病已经开始初步采用RNA干扰疗法。肿瘤治疗方面也已经取得了一些成果。














