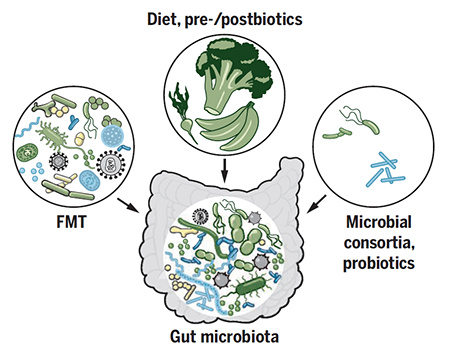
人体内有上万亿的微生物,它们对调节宿主的功能有着深远的影响。肠道内微生物的紊乱和许多疾病有关,包括神经系统疾病、心血管疾病、胃肠疾病甚至是癌症。因此,人们着眼于通过调整微生物群的来促进人体健康和消除疾病,并得了相当大的进展。调节肠道微生物策略包括粪菌移植(FMT),即将健康个体的粪便转移到另一个个体以获得预期的效果。粪菌移植以及其他肠道微生物调节方法在治疗几种疾病方面显示出良好的效果。
几个世纪前,古希腊医生希波克拉底(Hippocrates)就提出了胃肠道紊乱可能导致全身性疾病的观点。而最早报道使用FMT可以追溯到公元前4世纪的中国,通过粪便制剂治疗胃肠道疾病。而某些动物也采用类似的策略,通过食粪来增加肠道微生物多样性,并增强消化和其他生理功能。
1958年,FMT的第一次成功临床应用是用于治疗艰难梭菌感染(Clostridioides difficile infection, CDI)的伪膜性肠炎患者。
另外粪菌移植对于溃疡性结肠炎也有一定的效果,现在更多的临床实验正尝试把FMT和其他肠道微生物群调节策略推广到其他疾病上,例如治疗肠道疾病(如CDI和IBD)以及其他系统性疾病,包括代谢综合征、自闭症、多发性硬化症、帕金森病甚至癌症相关的临床试验已经进行。最新研究通过粪菌胶囊移植接合抗PD-1治疗转移性黑素瘤患者(单独抗PD-1治疗无效)并取得了良好的疗效。
肠道微生物的调节策略主要有两个方向:一是进行整个微生物群落的转移(通过FMT),其次是转移单一的微生物类群。但是,随着对肠道微生物功能的了解,更多的方法正在开发中。但是要实现对肠道微生物群的精确调节,还有很多工作要做。当考虑调借肠道微生物群的策略时,还需要考虑在目标人群的适应症。
在过去的几十年里由于抗生素的广泛使用,传染性疾病减少,但是过敏和自身免疫性疾病增加,也有部分原因是肠道微生物群的紊乱。通过调节肠道菌群可以治疗一些菌群严重失调的疾病(如CDI),而其他疾病也存在不同程度肠道菌群的破坏,因此选择合适的菌群调节策略还需考虑菌群失调的程度和特征。
在考虑调节肠道微生物群时,还应考虑许多因素,包括肠道微生物群调节方法和制备方案、测量肠道微生物和疗效的方法以及饮食的摄入等。一般来说,调节肠道菌群的目的是恢复患者健康的肠道微生物群落,但目前健康肠道微生物群的定义并不明确。有数据表明,具有高度功能冗余微生物群落与更好的健康和治疗结果有关。
FMT在治疗难治性CDI方面已展示出其安全性和有效性。正确的治疗指南和筛选供体粪便是安全的关键,包括筛查与肠道菌群紊乱相关的感染性疾病,以及药物的使用,如抗生素和质子泵抑制剂(PPIs)。目前,建议对供体进行多重耐药性微生物和新冠病毒 (COVID-19)的筛查。此前有报道称,数名CDI患者在FMT后出现全身感染,发生耐药性细菌感染并可能感染新冠病毒。粪菌菌移植的方式也很关键,大数据研究证实,肠菌胶囊和结肠镜下肠菌移植干预疾病疗效最显著。FMT供体中菌群的组成和功能可能会影响疗效,但是这种供体效应对于存在严重微生态失调的患者并不那么显著,例如CDI甚至IBD。FMT的最佳给药剂量和给药途径也不完全清楚,仍需要进一步研究。FMT的特性在于其提供的菌群多样性(不仅有细菌,还包括病毒、真菌和古生菌)有助于恢复菌群的功能冗余,但也存在可重复性等方面的局限,安全性、供/受体因素、剂量和移植途径等是FMT应考虑的因素。目前多项研究正在开发能够可靠、持续生产和管理的多菌株群落,用于良好的调节肠道微生物群,并提供比FMT更好的可扩展性。这些方法包括使用商业上常用的益生菌,然而多项微生物制剂治疗疾病的临床试验的结果不一。迄今为止,还没有被美国食品和药物管理局等主要监管机构批准使用的微生物制剂。下一代活的微生物治疗药物正在开发中与临床试验中,例如,2020 年 8 月 10 日,Seres 公司宣布了旗下肠道微生物组药物 SER-109 的 III 期临床试验结果,表明其可有效减少艰难梭菌感染复发风险,以及4D Pharma 公司宣布其活体微生物药物 MRx0518 与默沙东公司的免疫检检查点抑制剂 K 药(Keytruda)联用,在 I/II 期临床试验取得积极进展。在全球范围内,利用广义上属于益生菌的活菌药物辅助抗癌已成趋势,很快会有更多研究取得突破。尽管总体上这些微生物制剂的耐受性良好,但仍需考虑其安全性。有报道称,对危重患者使用益生菌来调节肠道微生物群时,这些微生物会从肠道进入血液中。
调节肠道微生物的其他重要因素是饮食和益生元,它们可以影响现有的共生肠道微生物和用于治疗的微生物。益生菌是一类对宿主有益的活性微生物,是定植于人体肠道、生殖系统内,能产生确切健康功效从而改善宿主微生态平衡、发挥有益作用的活性有益微生物的总称。人体有益的细菌或真菌主要有:酪酸梭菌、乳杆菌、双歧杆菌、放线菌、酵母菌等,商业层面上以乳杆菌和双歧杆菌为准。研究表明,饮食的巨大变化会在短期内对肠道微生物和相关生理反应产生显著影响。如果饮食上的改变没有持续下去,肠道微生物群可以恢复到干预前的状态。目前也有许多关于饮食干预的研究正在进行中,从简单的膳食干预(例如每天增加少量豆类,NCT02843425)到长期膳食干预(NCT03950635)。在膳食干预的同时进行FMT或者生物药物治疗,来观察膳食对维持和促进肠道微生物转移的作用,但是这些膳食干预的最佳方法尚未定义。一些可以作为有益共生微生物的底物,如益生元补充剂(如抗性淀粉、多酚和多不饱和脂肪酸)的使用也在研究中。单/多菌株的活菌药物,饮食/益生元干预及其与FMT或活菌药物的联合使用,也是临床研究热点。肠道微生物调节将越来越多地应用于促进人体健康和治疗疾病,尽管精确调节肠道微生物调节的最佳策略仍有待研究。调节肠道菌群的方法包括粪菌移植(FMT)、多菌株群落、饮食干预、益生菌/元和后生元等,在治疗一些肠道和系统性疾病上有一定效果,但没有普适性,在患者筛选、治疗方案、疗效评价标准、随访制度等方面存在很大差异,临床疗效和安全性也不一致。肠道菌群调节策略还需要进一步的研究和努力,更好地了解与疾病状态相关的肠道微生物群失调,以及促进整体健康的最佳肠道微生物群,对公共健康具有广泛的影响。[1] Modulating gut microbes. DOI:10.1126/science.abc3965